2. Tensioactive substances
Définition des tensioactifs
Les
tensioactifs, également appelés surfactants, ou molécules amphiphiles sont des
molécules qui comportent un tête hydrophile (polaire
ou chargée), et une queue hydrophobe de solubilité beaucoup plus faible dans
l'eau (Figure I-1). Grâce à cette double
solubilité pour les milieux polaires et apolaires, les
tensioactifs s'adsorbent aux interfaces. Cela
leur vaut d'être utilisés dans les formulations détergentes comme les lessives
ou les produits vaisselle afin d'éliminer la graisse ;
la partie hydrophobe du tensioactif peut s'attacher aux taches de graisse,
matériau hydrophobe. Lors du rinçage à l'eau, la partie hydrophile est emportée avec l'eau et la tache de graisse avec. Ces molécules sont également utilisées comme agent
moussant ou émulsifiant : en effet, ces molécules se
placent preferentiellement à la frontière entre l'eau et les milieux apolaires. Cette propriété leur permet de stabiliser les
émulsions et les mousses, ce qui représente un enjeu majeur
dans les domaines de la détergence et de la cosmétique. 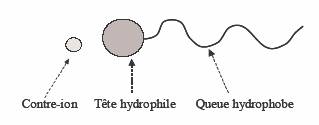
Figure - Structure of a tensioactive substance.
Il existe de nombreuses sortes de tensioactifs, qu'ils soient d'origine naturelle, (comme les phospholipides) ou synthétique (bien souvent des dérivés du pétrole). Parmi eux, on distingue les tensioactifs chargés et les tensioactifs non chargés. Les tensioactifs chargés comportent une tête ionique et un contre-ion de charge opposée, qui est dissocié dans l'eau. Il existe deux types de tensioactifs ioniques : les tensioactifs cationiques, dont la tête porte une charge positive (et un contre-ion négatif) et les tensioactifs anioniques, dont la tête est chargée négativement (et le contre-ion positivement). Il existe également des tensioactifs zwitterioniques, qui portent deux charges opposées sur la même molécule et les tensioactifs amphotères, dont la charge peut varier avec le pH. De même, si les tensioactifs les plus couramment utilisés ont une queue hydrophobe hydrocarbonée (composée d'une succession de -CH2-), il existe des tensioactifs a queue siliconée (-SiO(CH3)-) et fluorée (-CF2-). La structure chimique d'un tensioactif et le rapport des tailles et des solubilités de la queue et de la tête dans l'eau ou l'huile détermine ses propriétés aux interfaces et en solution.
I.A.1. Surfactants, surface tension, soap films
I.A.1.a Definition of surfactants and applications
The surfactants, called also tensioactive substances, or amphiphiles are molecules which posses a hydrophile head (polar or charged), and a hydrophobe tail with a lower solubility in water (figure I-1). Due to that double solubility in the polar and non-polar, the surfactants adsorb each other at the interface of the two types of media, as the interface water-oil or water-air. This is the reason why they are used in the formulae of detergents as lessive or vaisselle to eliminate the grease; the hydrophobic part of surfactants can attach the stain of grease, hydrophobic material. After rinsing with water, the hydrophile part is removed with water and the tail with grease. Those molecules are equally used as foaming agents or emulsifiers: these molecules place themselves preferentially at the surface between water and the apolar medium. This property allows them to stabilize the emulsions and foams, representing a major goal in the domain of detergents and cosmetics.
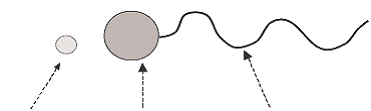
counter-ion hydrophile head hydrophobe tail
Figure I.1 Structure of a surfactant
There are numerous sorts of surfactants, which are of natural origin (like phospholipids) or synthetic (most often petroleum derivatives). Among them, we distinguish the charged surfactants and the charge-free surfactants. The charged surfactants are composed of an ionic head and a counter-ion of opposite charge, which dissociates in water. There are two types of ionic surfactants: cationic surfactants, who's head has a positive charge (and a negative counter-ion) and anionic surfactants, who's head is negatively charged (and a positive counter-ion). There are also zwitterionic surfactants, which bear two opposite charges on the same molecule and the amphoteric surfactants, who's charge can vary with the pH. Even if the most used surfactants have a hydrocarbonated hydrophobic tail ( composed of a sequence of -CH2-), there are surfactants with siliconed tail (-SiO(CH3)-) and fluorinated (-CF2-). The chemical structure of a surfactant and the relation between the size and the solubility of the tail and of the head in water or oil determine the properties at the interface and in solution.
I.A.1.b. Surface tension
The cohesion of liquids is insured by the intermolecular withdrawing forces of different nature ( Van der Waals forces, hydrogen bonds.) against which it has to rezist to maintain the molecule at the surface of a liquid. Creating an interface between two liquids has an energetic cost and for this reason, the interfaces have the tendency to minimize their aria. Imagining a system of volume V composed of two fluids separated by an interface of aria A. After a deformation dA of the interface, the Helmoltz free energy variation dF associated to that deformation can be written as:
![]() Eq. 1
Eq. 1
where S represents the enthropy of the system, T the temperature, P the pressure, V the volume, μ the chemical potential of the molecules and N their number. Also, at a constant number of moles, temperature and volume, the surface tension is defined as the free energy variation over the surface unit:
![]() Eq.2
Eq.2
To defining the surface tension as a function of free enthalpy, or Gibbs free energy, G, we must keep constant temperature, pressure and number of moles:
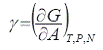 Eq.3
Eq.3
As we seen, the surface tension of a liquid can measure in any way its cohesion. Also, water, who's molecules are bonded by numerous hydrogen bonds has a high tension (72mN/m), in comparison with organic liquids as toluene (30mN/m).
3. Despre polielectroliti
Définition des polyélectrolytes
Un polyélectrolyte est un polymère porteur de charges électriques, et qui est, de ce fait, généralement soluble dans l'eau. A polyelectrolyte is a polymer which carries electric charges, and it is due to that, generally soluble in water. Les polyélectrolytes sont largement présents dans la nature (ADN, polysaccharides , mais aussi au niveau industriel (peintures, gels super absorbants,..).The polyelectrolytes are present in nature in a large amounts (DNA, polysaccharides, etc.), but also at industrial level (paints, super adsorbant gels, etc.). La compréhension des interactions de ces polymères avec d'autres substances chargées est un sujet d'actualité tant au niveau du fonctionnement des systèmes biologiques que de l'élaboration de matériaux à propriétés spécifiques.The understanding of the interactions of these polymers with other charged substances is a subject of present interest at the level of functioning of biological systems as in the elaboration of materials with specific properties. Les polyélectrolytes peuvent facilement se complexer avec des petites molécules tels que les surfactants et avec des macromolécules tels que les protéines.The polyelectrolyte can give complexe substances with small molecules, as surfactants, and with macromolecules, as proteins. Cette complexité conduit à différents types d'organisation moléculaires et supramoléculaires. This complaxation leads to different types of molecular and supramolecular structures.
Un polyélectrolyte est un polymère soluble dans l'eau. Ceci est utilisé pour:
A polyelectrolyte is a polymer soluble in water. For that reason it is used for:
Le développement des procédés "propres" qui remplace les solvants organiques des procédés classiques par des milieux aqueux,
Developing « peculiar » method which replace the organic solvents used in clasical methods with the aqueous media,
dans le traitement de l'eau,
wastewater treatment,
apporter au produit final des propriétés d'usage variées: agent stabilisant des mousses pour les produits cosmétiques, épaississants et gélifiants des produits alimentaires, rhéofuidification des peintures, stabilisants des suspensions colloïdales.
Confering to the final product multiple application properties : stabilizing agent of foams for the cosmetic products, thickening agents and gelifiers of food products, rheofluidization of paints, stabilizers of colloidal suspensions.
Un polyélectrolyte est un réservoir de charges électrostatiques. Il résulte :
A polyelectrolyte is a reservoir of electrostatic charges. It results:
un caractère extraordinairement hygroscopique - les supers absorbants sont des gels de polyélectrolyte,
a extrordinary hygroscopic character - the super absorbants are polyelectrolyte gels,
qu'on peut agir sur les polyélectrolytes avec un champ électrique et on utilise ceux ci en électrophorèse pour séparer des macromolécules en fonction de leur charge.
That it can be acted on a polyelectrolyte with an electric field and this can be used in an electrophoresis for the separation of macromolecules according to their charge.
Les chercheurs développent des polyélectrolytes amphiphiles qui adoptent des comportements associatifs qui leur confèrent des propriétés d'usage intéressantes. Researchers developed amphiphile polyelectrolytes which assume an associative behaviour which confer them interesting utilization properties. Les polyélectrolytes amphiphiles sont composés de deux sous unités: une ou plusieurs portions polyélectrolyte associées à des portions neutres hydrophobes (voir figure 1.1).The amphiphile polyelectrolytes are composed of two subunits: one or more polyelectrolyte's partitions associated with hydrophobic neutral partitions. On parle de:
It may be discussed of:
copolymère à blocs, lorsque ces sous unités s'enchaînent sous forme de bloc,
Bloc-copolymers, because their subunits are chained assume the shape of a bloc,
de polyélectrolyte modifié hydrophobe, lorsque des chaînes hydrophobes sont greffées sur un squelette de polyélectrolyte.
Hydrophobic modifyed polyelectrolytes, because the hydrophobic chaines are grafted on a polyelectrolyte's skeleton.
Dans les deux cas, les parties hydrophobes s'associent par "effet hydrophobe" pour diminuer l'aire des parties hydrophobes en contact avec l'eau en forme de: micelle, cylindre avec un coeur hydrophobe ou sous forme lamellaire. In both cases, the hydrophobic parts associate due to an "hydrophobic effect" to diminish the air formed as the hydrophobic parts make contact with water, in the form of: micelle, cylinder 121u2011b with a hydrophobic core or in lamellar shape.

Figure 1.1 - Les polyélectrolytes diblocs hydrophobes sont constitués d'un bloc polyélectrolyte et d'un bloc hydrophobe neutre qui forment en solution des assemblages supramoléculaires variés: micelles, cylindres, phases lamellaires et vésicules [2].
The dibloc hydrophobic polyelectreolytes are composed of a bloc polyelectrolyte and a neutral hydrophobic bloc which form in solution different supramolecular aggregates: micelles, cylinders, lamellar phases and vesicles.
Les polyélectrolytes interagissent fortement avec les objets de charge opposée. Les possibilités de mélanges sont: polyélectrolyte - surfactant, polyélectrolyte - polyélectrolyte, polyélectrolyte - protéine, polyélectrolyte - colloïde, polyélectrolyte - liposome et polyélectrolyte - cellule vivante. Dans tous les cas, les systèmes ont une tendance à former des assemblages plus ou moins bien définis et la compréhension précise de ceux-ci est souvent difficile.The polyelectrolytes strongly interact with the bodies of opposite charge. The mixing possibilities are: polyelectrolyte-surfactant, polyelectrolyte-polyelectrolyte, polyelectrolyte-protein, polyelectrolyte-colloid, polyelectrolyte-liposome, polyelectrolyte-living cell. In all the cases, the systems have a tendency to form aggregates more or less defines and their total understanding is quite difficult.
Le polyélectrolyte est une macromolécule contenant une fraction f non nulle de monomères ionisables. The polyelectrolyte is a macromolecule containing a fraction, f, not nule of ionisable monomers. On en représente comme un enchaînement de N monomères répartis en (1-f)N monomères neutres notés M et de fN monomères ionisables notés A- / B+, susceptibles d'être dissociés en A- et B+ (voir figure 1.3). It is represented as a concatenation of n monomers distributed in (1-f)N neutral monomers denotes M and fN ionisable monomers denoted A-/ B+, capable of dissociating in A- and B+ (see figure 1.3). M et A- / B+ s'enchaînent aléatoirement et deux paramètres suffisent à décrire un polyélectrolyte :M and A-/B+ concatenate aleatory and two parameters are enough to describe a polyelectrolyte:
N - longueur de la chaîne, nombre de monomères par chaîne,
N- lenght of the chain, number of monomers per chain,
f - taux de charge chimique, avec 0 < f
F- raport, indice, grad, coeficient of electric charge, with 0<f<1.
Si l'enchaînement des monomères ionisables le long de la chaîne se fait par les parties A-, on parle de polyélectrolyte anionique (voir figure 1.3).If the concatenation of ionisable monomers along the chain is made throu partitions A-, we speak about anionic polyelectrolyte ( see figure 1.3). Lorsque les charges se dissocient: When the charges dissociate:
il se forme un polymère de charge négative, appelé polyanion, et un grand nombre de cations simples, les contrions, se dispersent dans la solution,
it is formed a polymer with megative charge, called polyanion, and a great number of cations, the counterions, dispersed in solution,
il se forme un polymère de charge positive, appelé polycation, et un grand nombre d'anions simples, les contrions, se dispersent dans la solution.
It is formed a polymer of positive charge, called polycation, and a great number of simple anions, the counterions, dispersed in solution.
A partir de cette définition, on distingue plusieurs classes de polyélectrolytes. From this definition, we distinguish few classes of polyelectrolytes.
Lorsque f est faible, la présence de monomères ionisables, éventuellement dissociés, constitue une faible perturbation par rapport au cas neutre. When f is small, the presence of ionisable monomers, eventually dissociated, constitutes a weak perturbation compared with the neutral case. Forces de Van der Waals et électrostatiques sont en compétition. On parle de : Van der Waals and electrostatic forces are competing. We can talk about:
polyélectrolyte faiblement chargé, lorsque le taux de charge f est suffisamment petit pour que les forces de Van der Waals soient prépondérantes,
weakly charged polyelectrolyte, when the f is sufficiently small because the Van der Waals forces are preponderent,
polyélectrolyte fortement chargé, lorsque le taux de charge f est suffisamment important pour que les forces d'origine électrostatique soient prépondérantes,
strongly charged polyelectrolyte, when the f is sufficiently large because the electrostatic forces are preponderent.
Les polyélectrolytes faibles les plus courants sont des homopolymères constitués de monomères possédant une fonction acide faible ou base faible. The weak polyelectrolytes , most important the homopolymers constituted from monomers possessing a weak acidic or basic group.
Si la forme : If the :
basique portée par le polymère est chargée, le polyélectrolyte est anionique et l'affinité pour les protons se neutralise à mesure que le pH décroît.
Basic group of the polymer is charges, the polyelectrolyte is anionic and the affinity for protons is neutralised as the pH decreases.
acide portée par le polymère est chargée, le polyélectrolyte est cationique et d'autant plus dissocié que le pH est faible et cède des protons et se neutralise lorsque le pH augmente:
acid group of the polymer is charged, the polymer is anionic and dissociates as long as the pH is small and donates protons and is neutralised when the pH increasses.
Les polyélectrolytes forts ont le taux de charge indépendant de la composition du milieu. The strong polyelectrolytes have the f independent of the media composition. Les polyélectrolytes forts sont le plus souvent composés de monomères portant un groupe acide fort qui se dissocie totalement en libérant H+ ou des espèces salines de réactivité chimique nulle. The strong polyelectrolytes are usually composed of monomers carrying a strong acidic group which totally dissociates freeing H+ or alkaline species of nule chemical reactivity.
Il est important de remarquer qu'un polymère n'est pas intrinsèquement ionomère ou polyélectrolyte. It is important to notice that a polymer is not an intrinseque ionomer or polyelectrolyte. Seule l'interaction entre le solvant et le polymère va déterminer un comportement ionomère ou polyélectrolyte. Only the interaction between solvent and polymer will determine an ionomer behaviour or polyelectrolyte. Sachant que l'eau est le solvant le plus courant des polyélectrolytes, on distingue deux classes de polyélectrolytes :When water is used as solvent, we distinguish two classes of polyelectrolytes:
polyélectrolyte hydrophile: le polyélectrolyte est en bon solvant dans l'eau.
Hydrophile polyelectrolyte : the polyelectrolyte is a well solvated in water.
polyélectrolyte hydrophobe : le polyélectrolyte est en mauvais solvant dans l'eau.
Hydrophobic polyelectrolyte : the polyelectrolyte is not soluble in water.
Cette notion peut être généralisée dans le cas de polyélectrolytes solubles en solvant polaire différente de l'eau. This notion may be generalized in the case of polyelectrolytes soluble in polar solvents different from water. On parle alors de:Then we have:
polyélectrolyte solvophile lorsque le polyélectrolyte est en bon solvant,
solvophile polyelectrolyte when the polyelectrolyte is a good solvent,
polyélectrolyte solvophobe lorsque le polyélectrolyte est en condition de mauvais solvant.
Sovophobe polyelectrolyte when the polyelectrolyte is a bad solvent.
Par définition, un polyélectrolyte hydrophile plongé dans l'eau est solubilisé et libère un grand nombre de contreions. By definition, a hydrophile polyelectrolyte in water is solubilised and releases a great number of counterions. Deux interactions fondamentales sont ainsi mises en jeu : Two fundamental interactions are also very important:
interactions électrostatiques entre les charges, portées par le polymère et libres en solution
electrostatic interactions between the charges, carried by the polymer and released in solution,
interaction monomére-monomére à courte portée et connectivité à grande échelle
monomer-monomer interactions of short distance and connection at large scale.
Le régime dilué The diluted media.
Le « blob » électrostatique est utilisé pour décrire une chaîne polyélectrolyte isolée. The electrostatic "blob" is utilized to describe an isolated chain of polyelectrolyte. Pour une telle chaîne (polyélectrolyte linéaire), on introduit une longueur caractéristique, de ge monomères, à partir de laquelle l'énergie électrostatique à l'intérieur d'une chaîne est du même ordre de grandeur que l'énergie d'agitation thermique. For a such chain (linear polyelectrolyte), we introduce a characteristic length, of ge monomers, from which the electrostatic energy inside a chain is of same size order as the thermic agitation energy. On considère une chaîne gaussienne de taille xe, de ge monomères et ayant un taux de charges de f. We consider a Gaussian chain of size xe, of ge monomers and having a charge index f. On imagine maintenant une chaîne de plus grande masse, c'est-à-dire constituée de plus de ge monomères. Imagine a chaine of higher mass, being formed of more ge monomers. L'énergie électrostatique domine. The electrostatic energy dominates. La configuration gaussienne n'est pas stable et la chaîne s'étire sous l'effet des répulsions électrostatiques. The Gaussian configuration is not stable and the chain stretch under the effect of electrostatic repulsions.
Le modèle précédent prévoit une grande rigidité des chaînes polyelectrolytes. The previous model foresees an great chain rigidity of the polyelectrolyte. En effet une de formation de la chaîne a pour effet de diminuer la distance entre blobs distants. As the electrostatic forces are of long distance, the energy of the chain increases. Comme les interactions électrostatiques sont à longue portée, l'énergie de la chaîne croit. Ainsi, la chaîne sera rigide sur la distance des forces électrostatique. That is why the chain will be rigid along the electrostatic forces.
avec I la force ionique de la solution et lb la longueur de Bjerrum qui vaut 0,7 nm dans l'eau pur.
We can write the free energy of a polyelectrolyte as the sum of the component determined by electrostatic repulsions between monomers and the elastic component. Minimizing this energy proportionally to R, we find that the ray of chain varies linearly with the number of N monomers and increases exponentially with the effective charge ratio of the polyelectrolyte.
The similitude with the lather
law allows to show that the chain in diluted solution constitutes
electrostatic circles(globules) of diameter,![]() .
which corresponds to the length for which the thermic
agitation energy (kT) and the electrostatic energy compensate each other.
Inside a circle the chain has an ideal conformation. For the chains with higher
molecular weight, the circles grow electrostatically and have the tendency to
line up like a stick (Figure I-17-a).
.
which corresponds to the length for which the thermic
agitation energy (kT) and the electrostatic energy compensate each other.
Inside a circle the chain has an ideal conformation. For the chains with higher
molecular weight, the circles grow electrostatically and have the tendency to
line up like a stick (Figure I-17-a).
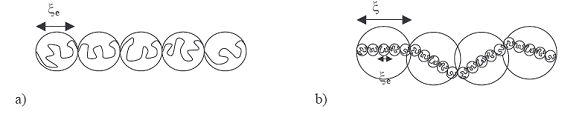
Figure I-17: a- stick(batonnete)
formed from electrostatic circles of dimension,![]() representing a polyelectrolyte chain in
diluted solution; b- concatenation of circles of dimension
representing a polyelectrolyte chain in
diluted solution; b- concatenation of circles of dimension![]() ,
containing electrostatic circles of dimension
,
containing electrostatic circles of dimension![]() .
.
After a
concentration c*, we enter the semi-diluted regime and the sticks start to
overlap. The solution is then composed of circles of dimension![]() ,
containing smaller circles of dimension
,
containing smaller circles of dimension![]() .
.
Le régime semi-dilué The semi-dilluted media
Note that the viscosity of semi-diluted solutions of polyelectrolytes increases with the charge ratio or with the length of the polyelectrolyte and decreases with the concentration of salt. Indubitable, the salt unscreens(blurs, blocks) the repulsions between charged monomers, which determines the collapse(breakdown) of the chain.
Lorsque la concentration augmente, les chaînes sont de plus en plus proches les unes des autres. When the concentration increases, the cahins are closer and closer to each other. La taille des chaînes devient comparable à la distance qui les sépare. Les chaînes ne sont plus isolées mais interagissent entre elles. The chains are no longer isolated and interact with each other. Au-delà de ces concentrations, elles peuvent s'interpénétrer. Beyond those concentrations, they can interpenetrate. Ce régime de concentration est appelé régime semi dilué. That regime of concentration is called semi-diluted. La longueur de Debye diminue lorsque la concentration augmente. The Debye distance decreases as the concentration increases. Les blobs d'une même chaîne subissent un écrantage mutuel. Toutefois les chaînes restent rigides sur une longueur, appelée longueur de persistance. Yet the chains remain rigid along a distance called propagation length. Dans le régime semi dilué, la longueur de persistance est très proche de la distance moyenne séparant des chaînes, x : l'espace peut être pavé d'une mer de blobs de taille x le. In the semi-diluted regime, the propagation length is around the average distance dividing the chains x: the space may be filled with a mer of blobs of size x le. La conformation d'une chaîne polyélectrolyte en régime semi dilué est illustrée sur la figure 1.3: elle se présente sous forme de bâtonnets de longueur lp librement joints et distants de x lp les uns des autres. The conformation of a chain of polyelectrolyte in semi-diluted media is shown in figure 1.3: it is presented as shot sticks of length lp.
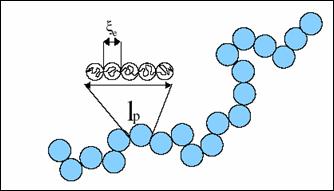
Figure 1.3 - Illustration de la conformation d'une chaîne polyélectrolyte
en régime semi dilué [1].
Illustration of the conformation of a polyelectrolyte chain in semi-diluted medium.[1].
Du point de vue des lois d'échelle :According to the power law:
at c = c*, 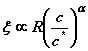 with c* the contact
concentration of chains; x is equal with the size of the chain, R;
with c* the contact
concentration of chains; x is equal with the size of the chain, R;
at c < c*, ![]() x is independent of R ;
x is independent of R ;
at c > c*, 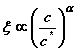 .
.
La dépendance de la longueur de persistance d'une chaîne polyélectrolyte avec la longueur de Debye se fait par deux approches différentes :The dependency of the propagation length of a polyelectrolyte chain on the Debye distance is done throu two different approaches:
according to Barrat and Joanny approach [6], the propagation lenght lp varies with k-1 ; this dependency expresses the fact that an intrinseque flexible chain remains flexible at small scales;
according to Odjik, Skolnick and Fixman' approach (OSF theory) [9], the propagation lenght lp varies with k-2 ; this law expresses that the electrostatic interactions make the chains rigid at every scale.
Les précédents modèles considèrent uniquement les répulsions électrostatiques dues aux charges portées par le macroion et ne considèrent pas le rôle des contre ions. The previous models consider only the electrostatic repulsions due to the charges of the macroion and not taking into consideration the role of the counter-ions. Or ceux-ci peuvent neutraliser certaines charges. Those can neutralize some charges. Ils peuvent se dissocier totalement du macroion (contre ions libres) et gagner de l'entropie en solution, ou bien rester associer à une chaîne (condensation), ce qui est favorable énergétiquement mais défavorable entropiquement. They may totally dissociate from the macroion ( free counter-ions) and gain the entropy in solution, or may remain associated to a chain ( condensation), which is energetically favorable but enthropically unfavorable.
On considère une solution de chaînes polyelectrolytes infiniment longues et toutes parallèles. Consider a solution of polyelectrolyte's chains infinitely long and all parallel. Autour des chaînes, il existe une surface équipotentielle où le potentiel électrostatique s'annule. Along those chains, there is an equipotential surface where the electrostatic potential is cancelled. Cette surface peut être approximée par un cylindre parallèle à la chaîne et d'épaisseur R. This surface may be approximated with a cylinder parallel to the chain and of thickness R. D'un point de vue électrostatique, chaque chaîne avec ses contres ions contenus dans le cylindre de rayon R, est indépendante des autres chaînes. From electrostatic point of view, each chain with its counter-ions contained in the cylinder of radius R, is independent of the other cahins. C'est donc un modèle de cellule avec une condition aux limites annulant le potentiel électrostatique à la distance R. It is a cellular model with boundary conditions canceling the electrostatic potential at distance R. Dans cette approche, la distribution des contres ions est continue et il n'y a pas d'état condensé proprement dit. In this approach, the counter-ion's distribution is continued and there is no condensation. L'espace se divise en deux régions : the space is divided in two regions:
une première région où l'énergie d'interaction entre les contres ions et supérieure à kT et où les contres ions sont donc liés à la chaîne ;
A first region where the energy of interaction between the counter-ions is higher then kT and where the counter-ions are tied to the chain,
une seconde région, plus loin de la chaîne où l'énergie d'interaction entre les contre ions et la chaîne est inférieure à kT et où les contre ions ne sont donc plus associés à la chaîne.
A second region, further on the chain where the energy of interaction between the conter-ions and the chain is smaller then kT and where the counter-ions are no longer attached to the chain.
Manning and Oosawa [8] used a model of two states. The counter-ions of a polyelectrolyte chain can self-condense on the chain, which is energetically favorable, or are dissociating in solution which is entropically favorable. The ions which are participating to condensation also allow screening the repulsions between the charged monomers. From this equilibrium, it results that the distance between two charges which dissociate successively is equal to the Bjerrum length, lb, which measures 7 A in water. For a vinylic chain, the minimal distance between two ionisable monomers is 2.5 A. If all monomers are ionisable, only a monomer of three is effectively charged so the 7 A length between two charges can be abided. It results that the effective charge ratio of a polyelectrolyte can not exceed 33% ionisable monomer content. This distance, lb represents the distance between two charges in a medium with the dielectric constant e for which the electrostatic energy between the charges is equal to the thermal agitation energy:
![]()
considering a the length of a monomer, is all monomers contain a ionisable group, only the free counter-ions contribute to the osmotic pression along the polelectrolytes chain.
Les contre ions sont soit associés à une chaîne soit dissociés. Ces auteurs ont prévu qu'un équilibre s'instaure entre les populations des ions libres et condensés, de sorte que la distance entre deux charges voisines du macroion est au minimum égale à la longueur de Bjerrum, lb. Cette longueur représente la distance séparant deux charges ponctuelles dans un milieu de constante diélectrique e, pour laquelle l'énergie électrostatique entre les charges est égale à l'agitation thermique :
![]() (1.2)
(1.2)
En appelant a la longueur d'un monomère, si tous les monomères portent un groupe ionisable, seuls les contres ions libres contribueront à la pression osmotique autour de la chaîne polyélectrolyte. La longueur de Bjerrum lb vaut 0 nm dans l'eau pure et a vaut 0,25 nm pour un polyélectrolyte carboné : cela conduit à une renormalisation des charges et à un taux de charge effectif de 30% (a/lb contres ions libres). En dessous de 30% de monomères portant un groupement ionisable, les contres ions seraient tous libres. Au dessus de ce seuil, le taux de charge effectif reste constant, tous les contres ions ajoutés restent liés à leur chaîne et sont donc condensés autour de celle-ci. According to the above said, the charge ratio remains constant, all the counter-ions remain attached to the chain and so are condensed to it.
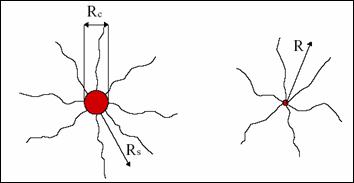
Figure 1.4 - Illustration d'une micelle (à gauche) et d'une étoile (à droite)
de polyélectrolytes en solution aqueuse. Les contres ions ne sont pas représentés [4].
Illustration of a micelle ( left) and of a star (right) of polyelectrolyte in aqueous solution. The counter-ions are not represented [4].
La figure 1.4 montre que ces micelles sphériques sont aussi des objets dont la configuration ressemble fortement à un colloïde sur lequel des chaînes polyelectrolytes sont greffées. The figure 1.4 shows that the round micelles are also bodies in which the configuration resembles with a colloid upon which the chains of polyelectrolytes are grafted. L'auto association en micelles des copolymères neutres - chargés dissymétriques résulte de la compétition énergétique entre le gain obtenu par les parties neutres dont la surface de contact est minimisée avec le solvant (mauvais solvant pour elles) et la pénalité imposée aux parties chargées à cause de leur extension et / ou des interactions électrostatiques et des contres ions.The self assembly in micelles of neutral copolymers- disymmetrically charged resulted from the energetical competition between the obtained energy by the neutral segments whose contact surface is reduced by solvent (weak solvent) and the penalty imposed to the charged segments due to their extension and/ or their electrostatic interactions and the counter-ions. La compétition énergétique n'était pas favorable à une association pour les copolymères fortement chargés et dissymétriques. The energetical competition isn't favorable for an association of strongly charged and disymmetrical copolymers. Marko et Rabin [9] considèrent une distribution de contres ions homogènes dans la micelle : ils ne prennent pas en compte la renormalisation des charges de la couronne et de la possible capture des contres ions le long des bras. Huang et collaborateurs [10] ont montré que la prise en compte de cette condensation était en faveur de l'association.
Par analogie avec les tensioactifs, l'association est prédite pour débuter au-delà d'une concentration appelée concentration micellaire critique, ccmc. En dessous de cette concentration, les chaînes sont toutes dissociées et la solution est similaire à une solution de chaînes linéaires. Au-delà de cette concentration, les chaînes ajoutées dans la solution, s'agrègent toutes et forment les micelles. La ccmc est prédite comme étant très faible. L'association en micelles sphériques de copolymères se faisaient pour des concentration aussi faibles que 2 10-8 à 2 10-7 g/ml. La ccmc définit la concentration de chaînes libres dans la solution. Elle ne varie donc plus lorsque la concentration en polymère augmente et ainsi, très rapidement, la concentration en chaînes libres dans la solution devient négligeable par rapport à la concentration en micelles. La détermination de la taille R et de Rc permet d'accéder à tous les paramètres structuraux d'une micelle. En effet, la différence entre R et Rc permet de déterminer Rs. De plus Rc est en fonction du nombre de chaînes, p, composant un objet. Ce dernier paramètre doit être nécessairement déterminé expérimentalement pour les micelles.
Interactions à l'intérieur des micelles et entre micelles
Dans le régime dilué c < c*
Les interactions entre bras chargés d'une micelle dépendent de la distribution des contres ions à l'intérieur de l'objet. Dans le cas d'étoiles polyelectrolytes de petite taille (quelque dizaine de nanomètres) et de faible nombre de bras ( 12), il a été observé des interactions entre bras. L'observation de ces interactions montre que les nuages de contres ions de chaque bras s'influencent les uns les autres. On peur attendre à observer de telles interactions dans la couronne des micelles.
Les interactions entre micelles dans le régime dilué dépendent de la capacité des couronnes à capturer leurs contres ions. Si une partie de contres ions libres n'est pas localisée à l'intérieur des micelles, il n'y a pas électroneutralité locale. Les micelles sont alors des objets chargés qui peuvent avoir des interactions électrostatiques entre elles, même à des concentrations inférieurs à c*. Ces interactions répulsives auront pour effet d'ordonner les solutions. A cause de l'extension radiale des chaînes de la couronne, la concentration en polymère de la couronne n'est pas constante avec r mais décroît hyperboliquement. Ainsi dans une brosse sphérique de faible nombre de chaînes, la concentration en polymère peut être très faible à la périphérie de la brosse. Il vient de suite que pour les cas où le nombre de bras sera faible, les couronnes auront du mal à capturer leurs contres ions. On peut donc s'attendre à avoir des interactions électrostatiques entre micelles dans le régime dilué lorsque les couronnes seront de faible densité une longue partie chargée et un faible nombre agrégation), tandis que pour les couronnes de plus grande densité, on peut attendre à ce que l'électroneutralité locale soit respectée et donc qu'il n'y ait pas d'interactions entre micelles avant c*.
Dans le régime concentré c > c*
L'étude des interactions entre micelles est très importante dans ce régime pour la modélisation du comportement des solutions colloïdales protégées par des polyelectrolytes.
Pour les étoile neutres aucun ordre entre objet n'a été observé avant c*. A c* un maximum d'ordre est observé et interprété comme un maximum de la pression osmotique Ensuite, au de la de c*, l'ordre disparaît, ce qui est interprété comme une interpénétration des micelles entre elles. Pour une micelle de forte densité (p ), un ordre apparaît bien à c* et persiste au-delà de c*. L'existence de cet ordre à de si hautes concentrations est incompatible avec une interpénétration des couronnes. L'interprétation des auteurs est une concentration des couronnes sans interpénétration de celle-ci. On cherche à étendre cette étude à des couronnes de plus faibles densités. Il semble raisonnable de penser que la densité de la couronne aura effet sur le comportement des micelles au-delà de c*. En effet, à cause de l'extension radiale des bras chargés, les couronnes peu denses pourront s'interpénétrer, sans changer la conformation de leur bras, c'est-à-dire sans apparition d'interactions entre bras : à la périphérie la concentration en polymère sera toujours faible. Il est aussi raisonnable de penser que, pour des nombres des bras intermédiaires, une interpénétration des couronnes peut avoir lieu comme pour les brosses sphériques neutres.
I.A.2. POLYMERS AND POLYELECTROLYTES
Polymers are molecules composed of a big number of key- units (N=10^@ to 10^6), called "monomers". When those monomers are charged, we refer to as polyelectrolytes. In pure state, the polymers are used for the manufacture of common objects as bottles for water (polyethylene terephtalate), polycarbonated glass, joints (siliconed polymers), tuyaux (PVC), or pare-chocs (polypropylene).In aqueous solution, polymers and polyelectrolytes are used for their rheologic properties as thickening agents and gelifiers, which makes them very useful in the cosmetics formulae or agro-alimentary. Polyelectrolytes are used as well for their adsorption properties at interfaces. The cationic polyelectrolytes are used in the shampoo formulae, because it can adsorb in to the hair and fortify it. We can assume that our body itself is composed of numerous polyelectrolytes molecules, as long as our DNA and all the proteins which compose our cells are also charged long-chain molecules.
Polyelectrolytes
Like repulsions between the charged monomers, the polyelectrolytes have a longuers de persistence much more higher then the neutral polymers. This results from the fact that the chains are more rigid and more expanded in space. Also, it requires low concentrations of polyelectrolyte because it is framed in the semi-diluted regime(medium).
Are distinguished strong polyelectrolytes, who's charges are fixed on the chain, like SO3- groups, weak polyelectrolytes, who's charges depend on the pH (-COOH groups). The charged monomer fraction is another key parameter which defines the polyelectrolyte.
Manning condensation
The counter-ions of a polyelectrolyte chain can self-condense on the chain, which is energetically favorable, or are dissociating in solution which is entropically favorable. The ions which are participating to condensation also allow screening the repulsions between the charged monomers. From this equilibrium, it results that the distance between two charges which dissociate successively is equal to the Bjerrum length which measures 7 A in water. For a vinylic chain, the minimal distance between two ionisable monomers is 2.5 A. If all monomers are ionisable, only a monomer of three is effectively charged so the 7 A length between two charges can be abided. It results that the effective charge ratio of a polyelectrolyte can not exceed 33% ionisable monomer content.
Structure in diluted and semi-diluted regimes
We can write the free energy of a polyelectrolyte as the sum of the component determined by electrostatic repulsions between monomers and the elastic component. Minimizing this energy proportionally to R, we find that the ray of chain varies linearly with the number of N monomers and increases exponentially with the effective charge ratio of the polyelectrolyte.
The similitude with the lather
law allows to show that the chain in diluted solution constitutes
electrostatic circles(globules) of diameter,![]() .
which corresponds to the length for which the thermic
agitation energy (kT) and the electrostatic energy compensate each other.
Inside a circle the chain has an ideal conformation. For the chains with higher
molecular weight, the circles grow electrostatically and have the tendency to
line up like a stick (Figure I-17-a).
.
which corresponds to the length for which the thermic
agitation energy (kT) and the electrostatic energy compensate each other.
Inside a circle the chain has an ideal conformation. For the chains with higher
molecular weight, the circles grow electrostatically and have the tendency to
line up like a stick (Figure I-17-a).
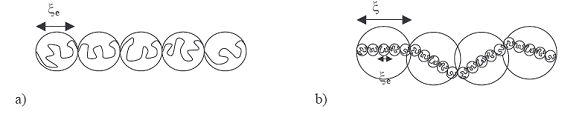
Figure I-17: a- stick(batonnete)
formed from electrostatic circles of dimension,![]() representing a polyelectrolyte chain in
diluted solution; b- inlantuire of circles of dimension
representing a polyelectrolyte chain in
diluted solution; b- inlantuire of circles of dimension![]() ,
containing electrostatic circles of dimension
,
containing electrostatic circles of dimension![]() .
.
After a
concentration c*, we enter the semi-diluted regime and the sticks start to
overlap. The solution is then composed of circles of dimension![]() ,
containing smaller circles of dimension
,
containing smaller circles of dimension![]() .
.
Note that the viscosity of semi-diluted solutions of polyelectrolytes increases with the charge ratio or with the length of the polyelectrolyte and decreases with the concentration of salt. Indubitable, the salt unscreens(blurs, blocks) the repulsions between charged monomers, which determines the collapse(breakdown) of the chain.
Polyelectrolytes in weak solvent
Different regimes have been studied, function of the salt concentration and the charge ratio of polyelectrolyte. The salt had the effect of modifying at the same time the interaction between the counter-ion and the monomer, and also the interactions between the charged monomers, the chains being able to adopt three different configurations: besides the pearls necklace configuration, the chains can assume the shape of globules, of "sausages", or they can maintain a stretched configuration.
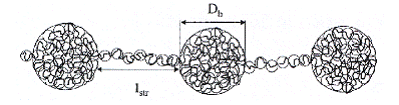
Figure I-18: Pearls necklace formed in solution by a chain of a hydrophobe polyelectrolyte
I.A.2.b. At interfaces
The adsorption of polymers and polyelectrolytes is of great practical interest: for example, a layer of adsorbed polymer can help decreasing the adhesion between two surfaces (coating a pan with Teflon), to stabilize the colloidal dispersions from steric repulsions between adsorbed chains (stabilization of cosmetic emulsions), or on the contrary for unstabilizing a dispersion (flocculation of polluting particles "by creating a bridge" for water treatment). So it is important to understand why and how the polymers adsorb themselves at interfaces. The case of polyelectrolyte is a lot more complex due to the fact that the short range forces, the effects of counter-ions and the multitude of parameters and interaction come out in the game.
The adsorption of polyelectrolytes at interfaces is a complex phenomenon, which depends on the charge of the surface, on the polyelectrolyte and on the salt concentration.
Generally, if the surface and the chains are of opposite charge, it exists adsorption. Otherwise, if the chains and the surface are of the same charge, they have the tendency to repulse themselves. In the case of a uncharged surface, there is a small attraction of the polyelectrolyte towards the surface, if it exists, of course, a chemical affinity between the monomers and the surface. For example, the hydrophobe polyelectrolytes have the tendency to adsorb at interface water-air and water-oil. The principal results concerning the adsorption of polyelectrolytes on a surface of opposite charge shows that the attraction of chains for the surface is screened by the presence of salt. More over, while the charge of the surface increases, the chain forms first of all a diluted medium (regime) then semi-diluted of two dimensions. Then, the chains start forming a self-similar grill of three dimensions, with tails which spread in the solution. When the solution becomes too charged, it becomes too constrained entropically for the chains to adsorb more monomers and some sites are replaced by counter-ions from the surface, which screen the attraction of chains for the surface. It results that the chains are separated from more monomers from the surface and that the thickness of the layer increases.
At weak ionic forces, the adsorption of polyelectrolytes over an uncharged surface is small because the chains don't exhibit affinity towards the surface and are good solvent in water. At high concentrations of salt, the chains are collapsing by themselves and can self-adsorb.
Adsorption of hydrophobe polyelectrolytes
There are many types of hydrphobe polyelectrolytes: The synthetic polyelectrolytes like the statistique copolymers or di- and tri- blocks, like modified polyelectrolytes with permanently hydrophobic tails. The diblocks and the triblocks are composed of charged monomers and of hydrophobe monomers. They can form micelles in solution. In the case of modified polyelectrolytes with permanently hydrophobic tails, the tails can form associations in solution and start (inbreed, engender) a network capable of thickening the solution. In a general way, the hydrophobe polyelectrolytes can self-adsorb at interface water-air if the number of hydrophobic entities is sufficient and the charge ratio is moderate. Based on the resemblance of these systems with our complexes polyelectrolyte-surfactant, we will describe the adsorption of the multiblocks copolymers and statistique copolymers.
Adsorption of the statistique "copolyelectrolytes"
Theory
As we've seen, the hydrophobe polyelectrolytes can form pearls "necklaces" and also globules in solution. These structures, more over the globules, are favorised at small charges ratio or at higher ionic force, because the electrostatic repulsions between chains are screened and the attractions between hydrophobe monomers become important.
Borisov showed that the adsorption of globules and pearl "necklaces" over a opposite charged surface is controlled by a balance between the electrostatic attraction of the chain towards the surface, the electrostatic repulsion between charged monomers and the surface energy of globules and pearls. While the ionic force increases or if the charge of the surface is weak, the globules are little attracted by the surface and remain spherical to minimize their surface energy. In certain cases, they can also disadsorb. If the surface is too charged, the globules squash (flatten) over the surface and form a pie-shape (Figure I-23).
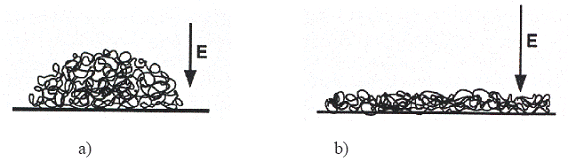
Figure I-23: a- adsorption of a globule of hydrophobe polyelectrolyte over an opposite charged surface. While the charge of the surface is weak the globule remains spherique. b- while the charge is higher the globule flattens itself to form a pancake.
In the case of pearls necklace, the pearls can also flatten if the surface is too charged. While the ionic force increases, these flattened pearls can coalescer and also desorber.
We distinguish three types of couples polymer-surfactant where the two species interact between themselves in aqueous solution :
When the dominating forces responsable for the interactions are clear enough for the last two categories, the driving force for the interaction inside the system neutral polymer- charged surfactant is less obvious. So, those systems arouse a great interest from theoretical and experimental point of view.
The critical aggregation concentration and chain saturation
In a system with fixed concentration in polymer in which are added increasing quantities of surfactant, Jones defined in 1967 two critical concentrations of surfactant to which we refer as CAC and X2 [ Jones, 1967]. The CAC, critical aggregation concentration is concentration from which appear the interactions between polymer and surfactant. Agreggation has here the meanning of formation of surfactant agreggates, in other words micelles linked to the polymer. X2 is the surfactant concentration for which the polymer is saturated in surfactant. These two concepts are essential for understanding and studying the interactions polymer- surfactant and are illustrated by the share stress curves.
In figure I.8 are reproduced the classic share stress curves of SDS solutions for differnt concentrations of PVP as function of SDS concentrations [Lange 1971 ou Purcell]. The essential characteristics of those curves are similar to those obtained for the system POE-SDS [Cabane 1977, Cooke 1998] and thus they summarize as : In presence of polymer, the share stress curve presents the two transitions mentioned plus haut at concentration CAC and x2. the concentration CAC represents the starting point in the formation of polymer- surfactant complexes. From this concentration it can be observed a constant (plateau) surface tension which reflects a constant activity of SDS molecules. That signifies that the surfactant monomers added along the plateau are consumed to form agreggates linked to the polymer until the chains are saturated with surfactant.From x2, the activity is constant meaning that in the solution are formed free micelles no longer linked to the polymer.
En présence de polymère, la courbe de tension de surface présente les deux transitions mentionnées plus haut aux concentrations CAC et x
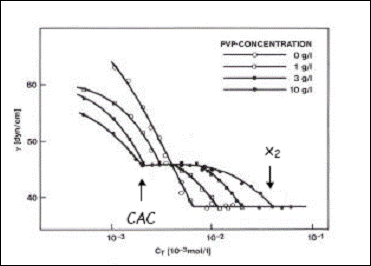
Figure I.8 : Surface tension of aqueous solutions of SDS for different concentrations in PVP [Lange 1971].
The figure I.8 shows that x2 increases with the concentration in polymer whereas the CAC is less sensitive to small quantities of polymer. In the case when the polymer itself if very tensioactive, as in the case of POP ( polypropylene oxide) and also PNIPAM, the results of surface tension for the mixed systems are difficult to interpret. La Figure I.8 montre également que x augmente directement avec la concentration en polymère alors que la CAC y est peu sensible sauf pour les très petites quantités de polymère.
Which is the driving force of the formation of complexes neutral polymers and hydrosoluble charged surfactant ?
Before taking an interest in the interaction polymer- surfactant, it is useful to consider first the self-assembly, namely the micellisation, of a classic ionic surfactant. The driving force for the assembly is the reduction of the contact area between water and the hydrocarbonated chains of surfactant. However, the micellisation results from a fragile equilibrium between many froces promoting or opposing the interaction. Particularly, the main force rezisting the agreggation is the electrostatic repulsion between polar charged heads when these last ones gather at the circumference of the micelles. The heavy density of charge resulting in that area will favorise the condensation of counter-ions to minimize the electrostatic potential and the repulsion between heads. Not only for geometrical restrains, it is important to keep the disposition ...........
Cependant, la micellisation résulte d'un équilibre délicat entre plusieurs forces favorisant ou s'opposant à l'interaction. En particulier, la force principale résistant à l'agrégation est la répulsion électrostatique entre têtes polaires chargées quand ces dernières sont rassemblées à la périphérie de la micelle. Ne serait-ce que pour des raisons de contraintes géométriques, il est important de garder à l'esprit que dans le modèle des micelles sphériques, la distance entre têtes polaires à la périphérie de la micelle est considérable à une échelle moléculaire. Une fraction de cette surface sera couverte de contre-ions mais une partie majoritaire sera constituée de chaînes hydrocarbonées exposées à l'eau, ce qui est une situation énergétiquement très défavorable (Figure I.9).
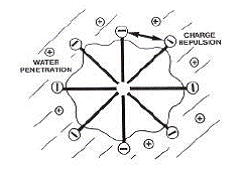
Figure I.9 : Représentation schématique d'une micelle de tensioactif anionique comme le SDS d'après Goddard [1993].
In consequence, all agents capable of reducing one and/ or other unfavorable interactions ( repulsions between the heads or great contact surface water- hydrocarbonated chains) will promote the micellisation. A first classical method is the introduction of salts which blocks the repulsions between heads and a second method is the addition of a cotensioactive substance of alcoholic type with short chain which will insert in the micelle.
Consider now a hydrosoluble neutral polymer composed of typical hydrophilic zones and hydrophobic regions. If the macromolecule is flexible enough, then it is possible to consider a configuration permitting at once a association ion-dipole between the ionic heads of the surfactant and the hydrophile part of the polymer chain and a contact between the hydrophobic regions of the polymer and the hydrocarbonated area of the micelle exposed to water. These configuration allows to block the electrostatic repulsions and diminish the hydrophobic area exposed to water. It is possible, due to the model of interactions between a neutral polymer and ionic surfactant developed by Ruckenstein et Nagarajan, to calculate the values of CAC of different systems from a certain number of parameters [Nagarajan 1979].
Structure des complexes polymère neutres-tensioactifs anioniques
Structure of neutral polymers and anionic surfactants
La structure permettant de relaxer une partie des deux contraintes décrites envisagée par différents auteurs est appelée structure de chapelet. The structure is composed of a macromolecule decorated with surfactant micelles (Figure I.10) [Shirahama 1974, Cabane 1977]. Cabane and Duplessix have studied using neutron diffusion at small angles the structure of POE-SDS complexes ( Cabane 1982,19985 and 1987). They deduced the stoechiommetry of necklesses and also different characteristic parameters corelated from polymer and surfactant point if view.
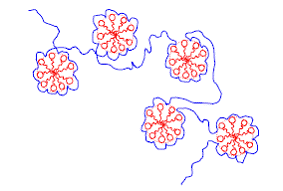
Figure I.10 : Schematic representation of the neckless structure.
Remarques sur la formation de complexes polymère-tensioactifs
Remarks over the formation of polymer-surfactant complexes
La formation de chapelets, c'est-à-dire de micelles de tensioactifs liées à la chaîne de polymère est énergétiquement plus favorable que l'autoassociation des molécules amphiphiles ce qui se manifeste dans une concentration d'agrégation critique (CAC) plus basse que la concentration micellaire critique (CMC).
The formation of necklesses, better said surfactant micelles tied to the polymer chain is more favourable energetically then the self-assembly of amphiphiles moolecules which takes place at a critical agreggation concentration (CAC) lower than the critical micellaire concentration (CMC).
Plusieurs conditions sont liées à la formation de la structure de chapelets :
For the formation of necklesses to take place there are few conditions :
-this structure requires a sufficiently long polymer chain with a flexible skelet ;
- the more hydrophobic the polymer is, the more it will interact with the surfactant ;
- the association with the surfactant is reinforced when, to the hydrophobic interaction is added an hydrophilic association. It is the case of PVP with anionic surfactants which contains a positively charged residue on each monomer which permits a strong electrostatic attraction with the polar heads of oppposite charge.
plus le polymère est hydrophobe et plus l'interaction avec les tensioactifs aura lieu tôt à la fois en termes de concentration en tensioactifs et de longueur minimale de la chaîne de polymère. Parallèlement, les macromolécules très peu hydrophobes comme le PAM interagissent peu avec les tensioactifs.

Figure III.1 : Schematic representation of configurations adopted by the polymer chains adsorbed or graphted over a surface.
The adsorption of polyelectrolytes is directed by hte electrostatic interactions and it depends strongly on the charge density at the surface and on the polymer chain and also on the salt concentration. Also the strongly charged polymers self adsorb too low or not at all in the case of a neutral surface. The addition of salt increasses the adsorbtion rate. Polyelectrolytes adsorb better on the oppositely charged surfaces.
The polymer behaves as a giant counter-ion for the surface and the enthropy increasses considerably when the chain of polyelectrolyte replaces the smaller counter-ions of the surface and frees in the same time it's own counter-ions. At a small salt concentration, this adsorption is very good and the polyelectrolyte chain sticks to the surface. A faible concentration en sel, cette adsorption est très forte et la chaîne de polyélectrolyte se couche à plat sur la surface.
The addition of salt reduces the interaction force and may cause the desorption of the polymer.
L'addition de sel réduit la force de l'interaction et peut provoquer la désorption du polymère.
If the formation of such complexes has done the object of many studies, their structure at interfaces and also the mechanism of adsorption and stabilisation of foams is still not very well understood. Our approach lead first to a study for the identification of the parameters which govern the polymer- surfactant interaction with a surface, and to determine how much they allow the modification of the characteristics of adsorption. As shown in the figure below, we studied the role of three parameters :
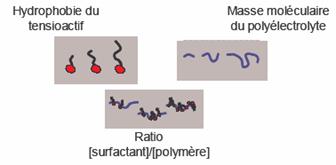
The hydrophobicity of the hte surfactant and the concentration ratios in polyelectrolyte and surfactant are two fundamental characteristics which allow to control the hydrophobicity of complexes formed and thus their solubility and also their affinity for the water-air interface. The molecular mass of the polyelectrolyte is a parameter which influences hte flexibility of the chains and their capacity of complexating surfactant molecules. To study those parameters, it was chossen to work with a system well charaterised, formed of a Prestol type anionic polyelectrolyte and a cathionic surfactant. And then with a Prestol type cathionc polyelectrolyte and an anionic surfactant. It was chosen a commercially Prestol having a small polydispersity index between 1 and few thounds of polyemers. The same way, the surfactants used were in pure state
In the first part of this work is presented a phase diagram of the surface. It was used the superficial tension by the stalagmometer method. As the adsorption of those complexes is very much influenced by their structure in solution there were also studied the interactions between polyelectrolyte and surfactant in solution with the help of a potentiometric technique using specific electrodes.
In the second part are studied the hreological prooperties of those complexes. For that, there were used two rheology techniques permitting the study of the answer of solutions when submitted to two types of constrains : normal forces and share stress. The rheological measurements were done with a co-axial cylindre viscosimeter and a con-plate viscosimeter. This approach allowed the determination of the rheological properties of solutions flowing under share stress and elongational stress.
Cette démarche on a permis de déterminer les propriétés rhéologiques des solutions en écoulement de cisaillement et en écoulement elongationel.
2. Rheology
The rheological characterisation of the polyelectrolyte solutions used in the treatement of wastewater makes the research subject for a better understanding of those materials.In the following is presented a review of the scientific literature works concerning the rheological caracterisation of polymers solutions, particularly polyelectrolytes.[1-25].
From ethymological point of view,rheology is the science which studies the flow, the deformation's of materials having undefined behaviour and intermediary between the perfect elastic behaviour of solids and the newtonian behaviour of fluids.
Newtonians Fluides
For the real fluids the superficial constrain has a tangential component ; is due to fluid viscosity. The constrain due to viscosity has for certain fluids a normal component, E (elastic effect),which adds up algebraically to the component .
Characterising the viscosity by mathematical models and determining the parameters of those models using experimental measurements.
Definig
from phenomenological point of view the tangential friction constrain by
![]()
The indexes y and x, recall that the constrain is takes place on the direction x along a surface on the direction y.Generally, the longitudinal rate gradient is called share rate gradient :
![]() gradient of
share rate.
gradient of
share rate.
Thus the relation will be written symbolically as:
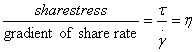 .
.
In the case of a newtonian
fluid, by definition, is
independent of ![]() and the diagram
connecting the share stress to the share rate gradient, called flowing curve or
rheogram is a straight line having the slope
(figure 2.1). All homogeneous fluids for which the diagram is a straight line
are called newtonian fluids.
and the diagram
connecting the share stress to the share rate gradient, called flowing curve or
rheogram is a straight line having the slope
(figure 2.1). All homogeneous fluids for which the diagram is a straight line
are called newtonian fluids.
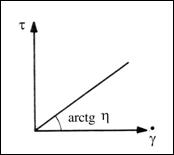
Figure 2.1 - the rheogram [2].
The newton law is a constitutive law. It bounds the deformation stress and the share stress, thus the flowing characteristics and the properties of the fluid.
Tenseur des contraintes
Consider a small element of volume dxdydz added up to volume forces ( inertia, gravity, etc.) applyed to the gravity center of the element and to the surface forces,soumis à des forces de volume (inertie, pesanteur..), resulted from the action of the environment upon the considered element, resulting dF.
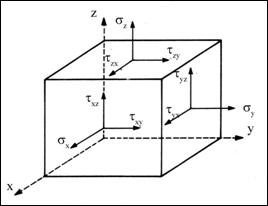
Figure 2.2 - Tenseur des contraintes [2].
The corresponding constrains upon the oriented faces of the paralelipiped must be defined in magnitude and on the direction of their projections in the coordinates direction. Defining thus a table of nine components which compose a second order vector:
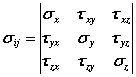
This tension is symmetrical,
thus ![]() . The share stress is chararcterized by six components.
. The share stress is chararcterized by six components.
The deformation stress and the flowing stress
The magnitude of deformations in a material is generally defined considering the relative infinitesimal displacement, so the difference of displacement in points M1 and M2 towards their initial gap.écartement initial.
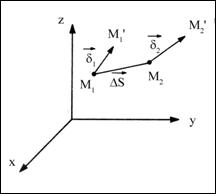
Figure 2.3 - Definition of the deformation stress [5].
The relative displacement is
denoted || and is 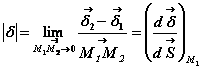
![]()
a trois composantes sur les axes x, y, z. To every one of those components corresponds three components of vector . Thus the relative displacement is a tensor having nine components according to the following sheme:
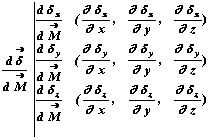
This tensor, ij, is the tensor of the displacement gradient ( the indexes i, j are the operators of a circular permutation on the coordinates x, y and z).
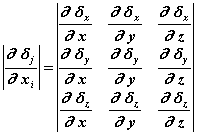
A component as the one
representing the relative displacement in the direction y, ![]() between two points
initially separated by dx in the direction x.
between two points
initially separated by dx in the direction x.
The
tensor (3.14) has two components: a symmetrical one eij and an
asymmetricall one rij being ![]() .
.
The tensor eij is called deformation tensor and describes the deformation of an element dx, dy, dz without rotation while the rij tensor is called rotation tensor and describes a rotation inside the element considered without deformation.
In the case of the solid materials, the displacement velocities are weak and the constrains are in direct relation with the deformations observed upon a short period of time, hence the definition of the displacement and deformation gradients.
In the case of
liquids which flow, on the contrary, such a definition is not adapted and is
used the deformation rate tensor. Effectively, to a deformation ![]() it corresponds a
deformation rate
it corresponds a
deformation rate 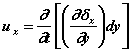 .
.
There by the displacement gradient tensor generates a deformation rate tensor:
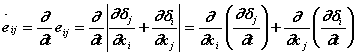 .
.
Beeing 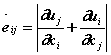 . A asymmetricall tensor ij also called vortex tensor
which represents twice the average rotation velocity of a fluid element:
. A asymmetricall tensor ij also called vortex tensor
which represents twice the average rotation velocity of a fluid element:
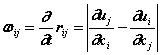
The tensor of the deformation rate may be decomposed in a symmetrical tensor and an asymmetrical tensor:
![]() ,
,
where ![]() ,the deformation rate is normal,
,the deformation rate is normal,
For an incompressible material ![]() , où
, où ![]() , where representes the share stress tensor very
important in the incompressible fluid mechanics.
, where representes the share stress tensor very
important in the incompressible fluid mechanics.
The classification of fluids according to their reological behaviour
The rheological classification
may be done according to the respective values of , , ![]() and according
to the time t corresponding to the duration of the eventual displacement.
and according
to the time t corresponding to the duration of the eventual displacement.
For the fluid state, are distinguished three main categories after the nature of the parameters which influence the shape of the flowing curve:
- fluids "independent of time" for which there is a
relation biunivocal between and ![]() . The fluids for which the relation =
. The fluids for which the relation = ![]() represents a peliculiar case of this type of fluids;
represents a peliculiar case of this type of fluids;
- fluids " dependent of time" for which the relation
between and ![]() depends on time and on the fluid mechanics;
depends on time and on the fluid mechanics;
- " viscoelastic" fluids which presents the characteristics of previous fluids and also of solids and parially get back in their initial shape after deformation.
Fluides non newtoniens au comportement indépendant du temps
For this type of fluids we may write the mathematical model as : ![]() , where the proportionality factor a is a value depending on
, where the proportionality factor a is a value depending on ![]() called apparent
viscosity.
called apparent
viscosity.
There are four main categories of fluids that are independent on time:
The fluids having a critical stress:
The plastic fluids of Bingham type,
The plastic fluids of Herschel-Bulkley type.
The fluids without critical strss of Ostwald de Waele type:
The pseudoplastic fluids or rheofluidified,
The dilatant fluids or les fluides dilatants or rhéoépaississants.
Fluids with critical stress
The plastic fluids are characterised in general by the flowing curves which can be represented by the relation of Herschel-Bulkley.
Generally, the flowing curve ends in a more or less liniar form from a maximum critical stress tc (figure 2.4). The slope extrapolated in origin gives the ordinate (Y-axis) and the flowinf relation may be written at first with approximation as :
![]() if > c
if > c
![]() = 0 if < c
= 0 if < c
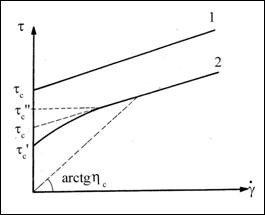
Figure 2.4 Rheoghrams of fluids having critical constrain [5].
If talking about Bingham fluids then the relation will be a good approximation of the fluid's behaviour. On parlera de fluide de Bingham lorsque la relation sera une très bonne approximation du comportement du fluide. c represents then theminimal level of constrains applied to a fluid for it to start flowing.
To explain the bingham behaviour of a fluid it can be assumed that it presents at rest a tridimensional structure, rigid, likely to resist at smaller constrains then c. If this constrain is superseded, the structure is being destroid and compromised the fluid to be newtonian under the effect of the effective constraint - c. If again the applied constraint becomes inferior then c the initial structure is being regained.
Table 1 reviews the pricipal laws of rheological flowing used to describe the behaviour of such fluids.
The Herschel-Bulkley model allows the description the majority of plastic fluids, the flowing curve of such fluids to become liniar from a certain critical constraint applied. The Bingham model is the simplest of those models, the Bingham fluids flow when a minimal level of constraint τB is est superseded. This model permits the description of hte rheological behavior of numerous materials (drilling mud, oil paints, some fats...).
Fluids without critical constraint
The flowing curves of the two main cathegories of fluids without critical constraint are shown in figure
Pseudoplastic fluids
Dilatant fluuids.
Table1 : Rheological models describing the flowing of fluids having a critical constraint
|
Model |
Rheological law |
|
Bingham |
|
|
Herschel-Bulkley |
|
|
General Casson |
|
|
Casson |
|
Pseudoplastic fluids
Their rheological behavior differs essentially from the
Bingham plastic fluids throu the fact that the pseudoplastic fluids do not show
the critical constraint of flowing. The ratio ![]() - apparent viscosity, is
at the begining close to the value of
- apparent viscosity, is
at the begining close to the value of ![]() , decreasing progresively when
, decreasing progresively when ![]() increases and the
flowing curve doesn't become liniar then for great values of . The boundary value of
the apparent viscosity a is then
named
increases and the
flowing curve doesn't become liniar then for great values of . The boundary value of
the apparent viscosity a is then
named![]() .
.
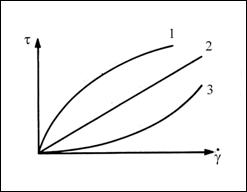
Figure 2.5 - Rheograms of fluids without critical contraint.
1.pseudoplastic fluids, 2. newtonian fluids, 3. dilatant fluuids [2].
Ostwald proposed for the representation of the flowing curves of those fluids the realtion named Ostwald-de-Waele law:
![]()
![]()
where k - consistency index of fluid
n - « flowing index »
the range between the exponent n
and the unity, translates the « viscous
imperfection » of the considered fluid. The model underlines very well
the fact that ![]() decreases when incrreses since n < 1.
decreases when incrreses since n < 1.
The rheological behaviour of those fluids is probably due to an orientation of the macromolecules advancing with the share rate in the way of flowing. At small the particles are perfectly disordered and at high values of , perfectly oriented, which explains the slightly newtonoan behaviour of those fluids at the boundary. On se saurait se contenter d'une explication aussi simple pour les solutions de macromolécules où on peut admettre la forte solvatation des molécules dans la dissipation. The increase of the share rate causes the graded destruction of the solvated bed. At small , the solvated bed is little modified and the interactions almost constant between molecules imply the liniarity of the flowing bed; contrary at high values of , This liniarity may be explained by the total destruction of solvated bed.
Dilatant fluids
These fluids obey also the « power law » of Ostwald but n > 1, in other words the apparent viscosity increases with . This type of behaviour was initial put in evidence by the suspension wiht lots of solid content. The dilatant fluids are fewer in Chemical Engineering than the pseudoplastic fluids. The main rheological laws describing the behaviour of such fluids are showed in table 2.2.
Viscous fluids dependent on time
It was shown the behaviour of previous fluids by their modifications in the internal structure. If those modifications are too fast, time does not interfer in any way in the flowing equations, on the contrary, if they are sufficiently nit the apparent viscosity mesure will depend on time. When there are disorganisations in structure by tearing, it is a thixotropic fluid, if there are organisations in structure, it is a rheopectic fluid.
Thixotropic fluids
The « consistency » of those fluids depends also on the share rate and on the time of share stress. If a tixotropic fluid is submitted to a stress after a period of rest, its structure is deorganized and it's apparent viscosity decreases in time. In proportion as the number of destroid bonds increases, the decreasing rate of the apparent viscosity diminuishes and the structure tends to reorganize itself at a rate which varies with the number of destroid bonds.
Table 2.2 - Rheological laws of fluids which do not have critical constraint [2].
|
Model |
Rheological law |
|
Ostwald de Waele |
|
|
Ellis |
|
|
Sisko |
|
|
Reiner Phillipoff |
|
|
Prandtl-Eyring |
|
|
Carreau |
|
|
Cross |
|
|
|
|
Figure 2.6 - Rheoghrams of thixotropic fluids [5].
At a given share rate, applied when t=0, after a long time of rest of the
fluid, we assist at a decrease of the tangential stress to a value of
equilibrium lower as ![]() is higher. (figure 2.6).
is higher. (figure 2.6).
The thixotropy iis a reversible phenomenon and at rest, the destroid structure reorganizes itself gradually. The figure 2.6 showes the evolution of the flowing curve of a thixotropic newtonian fluid according to the time of rest t before the starting of the experiment. If the flowing curve is drawn increasingly then decresing, there are obtained hysteres cycles schematically shown in figure 2.7. The size of the hysterese loop depends on the duration of the experiment.
|
a |
b |
Figure 2.7 - Rheoghram of thixotropic fluid [5].
It is very difficult to characterise experimentally the tixotropic or rheopectic fluids.It is very difficult to characterize by experiments the tixothropic fluids or the rheotropic ones. There are determined two curves : one Il est très difficile de caractériser expérimentalement les fluides thixotropes ou rhéopexes. On détermine une courbe d'écoulement de « montée » et une courbe de retour (figure 2.7b).
If we make vary proportionaly in time from O to we obtain the curve AB. si l'on fait varier proportionnellement au temps, de O à on obtient la courbe de montée AB.
si l'on fait décroître immédiatement , de à O on obtient la courbe de retour BCA,
si lors de la « montée », la vitesse de cisaillement est maintenue durant certain temps t, décroît suivant BD et la courbe de retour s'effectue selon DA.
si est maintenu durant un temps « infini », on atteint la position équilibre E et l'on obtient « la courbe de retour à l'équilibre » EA.
Rheopexes fluids
The rheopexy it is an extremely complex phenomena. Freundlich and Julius Berger showed that an aqueous solution of 42 % gyps is resolidifying in 40 minutes of rest after agitation, but in 20 seconds under the effect of a moderate share stress. In other words, for certain fluides call rheopex, an weak share stress is liable to favour the reconstruction of the fluid, but above a critical value, there are modifications in the structure. La rhéopexie est un phénomène extrêmement complexe et qui a été étudié que de manière qualitative. Freundlich et Julius Berger ont montré qu'une solution aqueuse de gypse à 42% se resolidifiait en 40 minutes au repos après l'agitation, mais en 20 secondes sous l'effet d'un cisaillement modéré. Autrement dit, pour certains fluides dits rhéopexes, un faible cisaillement est susceptible de favoriser la restructuration du fluide, mais au-dessus d'une valeur critique, il y a désorganisation de la structure.
Viscoelastic fluids
A viscoelastic fluid is a fluid which posesses viscous and elastic properties.
Consequences of viscoelasticity over the behaviour of the fluids
consequences of share stress
When a fluid is flowing throught a tube under the difference of pressure (p1 - p2), it establishes a parabolic profil of velocity when the forces of viscosity prevail. In stationary regime, if the viscosity of a newtonian fluid and of a viscoelastic fluid are identical, then they will have the same profil of velocity in the tube for the same flow rate. The profil of the velocity cand be seen better by repacing, at t = 0, the initial fluid with acolored one which moves through the tube containing a parabolic shape. If the rate flow stops at t > 0, Lorsqu'un fluide s'écoule dans un tube sous la différence de pression (p1 - p2), il s'établit un profil de vitesse parabolique lorsque les forces de viscosité prédominent. En régime stationnaire, si la viscosité d'un fluide newtonien et d'un fluide viscoélastique et identique, on a le même profil de vitesse dans le tube pour le même débit. Le profil de vitesse peut être traduit visuellement en remplaçant, à t = 0, le fluide initial par un fluide coloré qui progresse dans le tube avec un front parabolique. Si le débit cesse à t > 0, ce front se conserve pour un fluide newtonien alors qu'il se rétracte pour un fluide viscoélastique par suite de la récupération élastique (figure 2.8a). On conçoit les problèmes que peut poser ce phénomène lors des écoulements transitoires (vannes de réglage, extrudeuses...).
|
a |
B |
Figure 2.8 - Effets de viscoélasticité en écoulement [5].
We will consider the same fluids submited to stress between a plate and a cone. At t= we apply a torque C which inhibits it at t > 0 . W will see an angle of deformation (t). The angle will finaly take an asimptotic value for a viscous fluid continuing in a monotone way with t . A viscoelastic fluid can present oscialationsdue ti it's elasticity figure 2.8b). On considère ces mêmes fluides soumis à cisaillement entre un plateau et un cône. A t =0, on applique un couple C que l'on supprime à t > On observera un angle de déformation (t). L'angle finira par prendre une valeur asymptotique pour un fluide visqueux en évoluant de façon monotone avec t. Un fluide viscoélastique pourra présenter des oscillations amorties dues à son élasticité (figure 2.8b).
Consequences of normal stress: Weissenberg effect
The viscoelastic fluids also show normal stress anisotrop also in a state of simple share. The consequence of this normal stress is called Weissenberg effect. Les fluides viscoélastiques ont la propriété de présenter des contraintes normales anisotropes même dans un état de cisaillement simple. La conséquence de ces contraintes normales est appelée effet Weissenberg.
|
a |
b |
c |
Figure 2.9 - Viscous effect in flow [2].
If we submit a fluid to a rotation force driven by a rotating cylinder in a laboratory glass ( figure 2.9a), it will form a vortex in a viscous fluid, under the influence of the centrifuge force. The viscoelastic fluid develops orthogonal share stresses at tangential share stress and climbs along the rotor. Si on soumis un fluide à une rotation forcée entraînée par un cylindre tournant dans un bêcher (figure 2.9a), il se développe, sous l'influence de la force centrifuge, un vortex concave dans un fluide visqueux. Le fluide viscoélastique développe des contraintes de cisaillement orthogonales aux contraintes de cisaillement tangentielles et grimpe le long du mobile.
Also a fluid jet passed through an orifice is contracting under the effect of acceleration due to gravitation ( it's own weight). A viscoelastic fluid will present a relaxation and enlargement of the jet due to the orthogonal constraines and to the share stress (figure 2.9b).
Lets consider a disk, having a rotative orifice, placed above a flat disk. For a viscoelastic fluid we will see a reversed flowing in comparisson with the situation observed for a viscous fluid (figure 2.9c).
Du même un jet issu d'un orifice se contracte sous l'effet de l'accélération due à la pesanteur. Un fluide viscoélastique va présenter au contraire un ralentissement et un élargissement du jet dû aux contraintes orthogonales et aux contraintes de cisaillement (figure 2.9b).
On considère un disque percé d'un orifice tournant au-dessus d'un disque plein. On assistera pour un fluide viscoélastique à une inversion de l'écoulement par rapport à la situation observée pour un fluide visqueux (figure 2.9c).
Linear viscoelasticity.
A viscoelastic fluid recovers a part of its deformations after it is subjected to constrains and the constrain associated to a deformation diminueshes in time.The behaviour of the viscoelastic fluids can be described as the resultant of the association of strings and bumpers. All the associations between strings and bumpers correspond to a linear viscoelastic behaviour. Starting from the law of association in series or in parallel, we can establish the rheological equation of every model and deduce the flowing and relaxation functions in every particular case. It is known that the Kelvin- Voigt and Maxwell models generalize enough for that deduction without the flowing and relaxing functions.The Maxwell model corresponds to the association in parallel of n Maxwell fluids, each of them being made of a string and a bumper in series. The Kelvin- Voigt general model is made by the association in series of a Maxwell fluid and n Kelvin- Voigt solids (itself being made by association in paralle of a string and a bumper).
Un fluide viscoélastique récupère une partie de ses déformations après suppression des contraintes et la contrainte associée à une déformation, diminue dans le temps Le comportement viscoélastique de fluides peut être décrit conceptuellement comme résultant de l'association de ressorts et d'amortisseurs. Toutes les associations de ressorts et d'amortisseurs, aussi complexes soient-elles, correspondent à un comportement viscoélastique linéaire. A partir des lois d'association en série et en parallèle, on peut établir l'équation rhéologique de chaque modèle et en déduire les fonctions fluage et relaxation dans chaque cas particulier. Il s'avère toutefois que les modèles de Kelvin-Voigt et de Maxwell généralisés suffisent pour déduire n'importe quelles fonctions de fluage et de relaxation. Le modèle de Maxwell correspond à l'association en parallèle de n liquides de Maxwell, chacun d'eux étant constitué par un ressort et un amortisseur en série. Le modèle de Kelvin-Voigt généralisé est pour sa part constitué par l'association en série d'un liquide de Maxwell et de n solides de Kelvin-Voigt (constitué lui-même par l'association en parallèle d'un ressort et d'un amortisseur).
The general relation of the viscoelastic behavior :
![]() .
.
Examples of Kelvin-Voigt solids with τ = τo = cte for t >> 0 and γ = 0 for t <
![]()
Where λ = µ / G
The relaxation time corresponds to the value λ while the tension γ decreases to 1/e from it's initial value.
If t >> λ
(t) = τ.J∞ + τ.t/µ
Le temps de relaxation correspond à la durée de valeur λ pendant laquelle la tension γ diminue de 1/e de sa valeur initiale.
Si t >> λ
(t) = τ.J∞ + τ.t/µ
The flowing functions J(t) and relaxation G(t) characterise the flowing of the viscoelastic fluids just like in the simple stress model. The similation of those functions, genrally brings to equations of this type : (t) = J(t).τ + O(τ3).
Les fonctions de fluage J(t) et de relaxation G(t) caractérisent l'écoulement des fluides viscoélastiques selon les modes de mesures en cisaillement simple. La modélisation de ces fonctions conduit généralement à des formes développées du type γ (t) = J(t).τ + O(τ3).
The corresponding viscoelastic propertis are not Les propriétés viscoélastiques correspondantes ne sont donc pas aisées à déterminer et leur caractérisation ne fournit pas de paramètres clés rapidement identifiables. Moreover, the method of loading torque De plus, la méthode de sollicitation en cisaillement simple repose sur des échelons de contrainte (fluage) ou de déformation (relaxation) imposés de façon instantanée. In fact, this theoretic principle is compared with the mechanic inertia of the measurement system of the rheometers.That is why we use the oscilatory response of the viscoelastic fluids submited to sinusoidal solicitations as function of time. En réalité, ce principe théorique est confronté à l'inertie mécanique du système de mesure des rhéomètres. C'est pourquoi on utilise les propriétés de réponse oscillatoire des fluides viscoélastiques soumis à des sollicitations de type sinusoïdales en fonction du temps.
Le comportement rhéologique particulier des solutions de polyelectrolytes. The peculiar rheological behaviour of polyelectrolyte solutions.
In a dilluted solution which flows, the conformation of an unique chain is dynamic.The behaviour of a chain is modified by the persence of a solvent and other chaines. In a good solvent a chain of polyelectrolyte is behaving as sugested in the figure So if a chain is in a « good solvent », the solvent which likes the contact with the chain has the tendency to « swallow » it. Dans une solution diluée en écoulement la conformation d'une chaîne unique est dynamique. Le comportement d'une chaîne est modifié par la présence du solvant et d'autres chaînes. Dans un bon solvant la chaîne du polyélectrolyte se comporte comme suggère la figure 2.10: Lorsqu'une chaîne est dans un «bon solvant», le solvant qui aime le contact avec la chaîne à tendance à la «gonfler»

Figure 2.10 - The polyelectrolyte micelle in a good solvent [9].
The solution gains energy due to the contact between the chain and the solvent and looses enthropy through the « swallowing » of the chain. The compromise gives a low of exponentially increassing distance/different lenght : R0 = lK(L/lK)0.6 . It results that increasing the surface with lenght is faster. Increasing the concentration the chains are entangling and it is obtained the semi-diluted regime. La solution gagne énergie avec les contacts chaînes/solvant et perde entropie par le «gonflement» de la chaîne Le compromis donne une loi de croissance distance bout à bout/longueur différente: R0 = lK(L/lK)0.6 Il résulte que l'augmentation de taille avec la longueur est légèrement plus rapide. En augmentant la concentration les chaînes s'enchevêtrent et on obtient le régime semi-dilué.
A polymer chain it is an object submited to a Brownian agitation which generate a change in configuration. It takes the shape of a ball which is a lot smaller than it's normal lenght and it resists through an elastic recovery to all forces (elasticity). It's moves are very slow ( moreover if they are entangled). It is the elasticity of the chaines and their dynamics which will determine the mechanic properties of the systems. Une chaîne polymère est un objet soumis à une agitation Brownienne qui la fait changer de configuration. Elle constitue une pelote qui est beaucoup plus petite que sa longueur étirée et résiste par une force de rappel à tout étirement (élasticité). Ses mouvements sont très lents (surtout si elle est enchevêtrée). Ce sont l'élasticité des chaînes et leurs dynamiques qui vont déterminer les propriétés mécaniques des systèmes.
In general, if a system is deformed instantaneous, this forgets it's initial structure. So, if a degree of friction is applied of about x s- the initial structure is irreversibly destroied in 1/x seconds. If a system has a natural relaxation time equal with tr, then if it is applied a share stress equal to à tel que très t grande devant 1, the system has no time to relax and it's structure is deeply affected by the stress (see figure 2.11 and 2.12). En général, lorsque l'on déforme instantanément un système, celui-ci oublie sa structure initiale. Donc si l'on applique un taux de cisaillement de x s-1, on « efface » l'histoire en un temps de 1/x seconde. Si un système a un temps de relaxation naturel égal à tr, alors si on applique un cisaillement égal à tel que très t grande devant 1, le système n'a pas le temps de relaxer et sa structure est profondément affectée par le cisaillement (voir la figure 2.11 et 2.12).
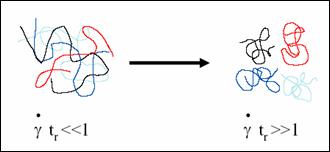
Figure 2.11 - The signification of the relaxation time [8].
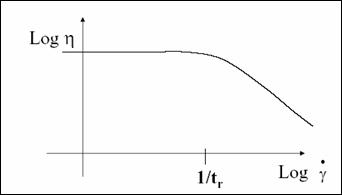
Figure 2.12 - The signification of the relaxation time in a rheoghram
When a deformation is applied to a solid body, it responds often through a constrain proportional to the imposed deformation, it is called Hooken solid. Then:t = Gγ, G is called elastic module. It has the same measurement unit as the constrain. Lorsque l'on applique par contre à un corps solide une déformation, celui-ci répond souvent par une contrainte proportionnelle à la déformation imposée, on l'appelle solide Hookéen. On a donc :t = Gγ, G est appelé le module élastique. Il a la même unité que la contrainte.
The rheology is controled by : the elastic model (au plateau ou au temps court) and the relaxation time of the constrain. The viscosity is the product of two quantities. The precise analysis of phenomena revised through the study of the viscoelastic module. Each deformation induces a constrain which will : add to the previous ones and relax (independent of other constraines). La rhéologie est contrôlée par : le module élastique (au plateau ou au temps court) et le temps de relaxation de la contrainte La viscosité est le produit des deux quantités L'analyse précise du (ou des) phénomène(s) passe par l'étude du module viscoélastique. Chaque déformation induit une contrainte qui va.s'additionner aux précédentes .et relaxer (indépendamment des autres)
The thermodynamic constraines (elasticity of short time) dominate the weak state of stress.They create the viscoelasticity. The constrain of hydrodynamic origin (flow of the solvent) dominate the strong state of stress. Les contraintes d'origine thermodynamique (élasticité au temps courts) dominent à faible taux de cisaillement. Elles créent la viscoélasticité. Les contraintes d'origine hydrodynamique (écoulement de solvant) dominent aux forts taux de cisaillement
The rheological behaviour of aqueous solution of semi-diluted polyelectrolytes. Comportement rhéologique de solution aqueuse de polyélectrolytes semi-dilué.
The solutions are non-newtonian fluides. Four types of distinct behaviour are presented below. Les solutions sont des fluides non-newtoniens. Quatre types de comportement distincts sont référencés dans la bibliographie, ceux-ci font l'objet d'une présentation dans la partie qui suit.
Pseudoplastic behaviour Comportement pseudoplastique.
A rheofluidifiant fluid sees it's viscosity decreasing with the incresing of the share stress, the liquid becomes less viscous and so more fluid when the share stress increasses. The Ostwald and Sisko models are more often used for describing the rheologic behaviour. Schurz [1] shows that the flowing indices n of the Oswald model increases with the concentration in polyelectrolyte, meaning that the fluidizing character becomes more obvious with the increase of concentration. Montreux [14] determine the coefficients of a model similar to Oswald's model which describes directly the apparent viscosity as a function of the velocity gradient for the Praestol solutions and reviews the modelation providing the best possible correlations for describing the flow of these solutions. Un fluide rhéofluidifiant voit sa viscosité décroître avec le cisaillement qui augmente, le liquide devient moins visqueux et donc plus fluide lorsque le cisaillement croît. Les modèles d'Ostwald et de Sisko sont les plus souvent utilisés pour décrire le comportement rheologique. Schurz [1] montre que l'indice d'écoulement n du modèle d'Ostwald augmente avec la concentration en polyélectrolyte, c'est-à-dire que le caractère fluidifiant de la devient plus évident avec l'augmentation de la concentration. Montreux [14] détermine les coefficients d'un modèle similaire à celui d'Ostwald qui décrit directement la viscosité apparente en fonction du gradient de vitesse pour les solutions de Praestol et recherche la modélisation fournissant les meilleures corrélations possibles pour décrire l'écoulement de ces solutions.
The plastic behaviour Comportement plastique.
The plastic behaviour of the Praestol solutions is also marked by a high concentration in polyelectrolyte [8]. The Bingham and Herschel-Bulkley models are the most relevant to describe their rheological behaviour. The definition of the flowing limit of the solution remains very different according to the studies. Le comportement plastique des solutions de Praestol est d'autant plus marqué que la concentration en polyélectrolyte est élevée [8]. Les modèles de Bingham et de Herschel-Bulkley sont alors les plus employés pour décrire leurs comportement rhéologique. La définition du seuil d'écoulement de la solution reste très différente selon les études considérées.
The thixotropic behaviour Comportement thixotrope.
The tixothropy
shows the importance of the mechanical history of materials in the
determination of their rheological behaviour. A thixothropic fluid posesses in
general, a rheofluidifying character which is manifested by a decreasing in
viscosity therefore increasing the value of the share stress [21 ]. The effects of this fluidyzation
doesn't appear entirely therefore they may differ in time. The induced
destruction is manifested in a different manner, which is read by the help of
rheograms resulting from the linear increase and decrease of the stress
velocity which are asimetric, the decreasing curve is placed below the
increasing curve of the stress velocity. The concentrated Praestol solutions
are reported as being fluids presenting thixothropic properties [21 ]. La thixotropie témoigne de l'importance de l'histoire
mécanique antérieure du matériau dans la détermination de son comportement
rhéologique. Un fluide thixotrope possède en général
un caractère rhéofluidifiant qui se manifeste par une diminution de la
viscosité lors de la montée en vitesse de cisaillement [21, 24]. Les effets de
cette fluidification ne se produisent pas en totalité lors de l'application du
cisaillement mais peuvent être différés dans le temps. La déstructuration
induite par le cisaillement se manifeste de façon différée, ce
qui se traduit par des rhéogrammes résultant de montée et descente linéaire en
vitesse de cisaillement qui sont asymétriques, la courbe de descente se situant
en dessous de
The viscoelastic behaviour Comportement viscoélastique.
The Praestol solutions in semi-diluted are viscoelastic, in other words they have in certain conditions similar characteristics to the elastic corps (non fluids) and in other conditions they have the characteristics of simple viscous fluids[1,4]. More precise, when a constrain is applied the time must be very short, their response is elastic, in other words the resulted deformation is proportional with the applied constrain. If a solicitation is applied for longer time then the response is viscous, in other words that it is flowing sooner than producing a deformation. Gleissle showed that the viscoelastic solutions which produce oscillations during the measurement of the rheological characteristic in a con- plate viscosimeter have a difference of second order N2 positive. Les solutions de Praestol en régime semi-dilué sont viscoélastiques, c'est-à-dire ont dans certaines conditions des caractéristiques analogues à celles de corps élastiques (non fluides) et dans d'autres conditions des caractéristiques de fluides simplement visqueux [1, 4]. Plus précisément, lorsqu'une sollicitation leur est imposée pendant une durée très courte, leur réponse est essentiellement élastique, c'est-à-dire que la déformation résultante est proportionnelle à la contrainte appliquée. Par contre, lorsqu'une sollicitation leur est imposée pendant une durée assez longue, leur réponse est essentiellement visqueuse, c'est-à-dire qu'ils s'écoulent plutôt qu'ils ne se déforment. Gleissle et les collaborateurs [19] ont montré que les solutions viscoélastiques qui produisent des oscillations pendant le mesurage de la caractéristique rhéologique dans un viscosimètre con - plaque ont la différence de deuxième ordre N2 positive. La plus part des polymères ont cette différence négative. C'est le cas des solutions de Praestol.
Bibliographie
J. Schurz - Prog. Polym. Sci, 16, p1, 1991.
M. Mihai - « Mécanique des Fluides en Génie Chimique », UPB, 1994.
L. M. Ion, D. S. Vasilescu, C. Cincu - « Composés Macromoléculaires II Physique des Polymères mise en Oeuvre des Polymères », UPB, 1995.
C. W. Mascosko - Rheology : Principles, Measurements and Applications, Weley VCH 1995.
Midoux, N. - « Mécanique et Rhéologie des fluides en génie chimiques », Technique et documentation, Paris, 1985 et édition 2000.
C. Cincu, L. M. Butac, I. Stancu, M. Clemens - Rhéologie et mise en ouvre des polymères, Ed. Printech, Bucuresti, 2002.
M. Mihai, I. Pincovschi - « Mécanique des Fluides Appliquées », Ars Docenti, 2005.
C. Esquenet - Thèse de doctorat de l'Université Joseph Fourier Grenoble, 2003.
N Tixier - Thèse de doctorat de l'Université de Limoges, 2003.
L. Li, R. Larson - Rheol. Acta, 39, p419, 2000.
V. F. Kurenkov, S. V. Snigirev, F. I. Churikov, A. A. Ruchenin, F. I. Lobanov - Russian J. of Appl. Chem, 74, p445, 2001.
J. C. Majecté, A. Allal, J. P. Monfort - Rheol. Acta, 42, p477, 2003.
Y. R. Jeng, C. C. Chen, S. H. Shyu - Tribology Letters, 15, p293, 2003.
C. Monteux - Thèse de doctorat de l'Université Paris VI, 2004.
G. Fleury, G. Schlatter, R. Muller - Rheol. Acta, 44, p174, 2004.
J. L. Viota, J. de Vicente, M. M. Tejada, J. D. G. Duran - Rheol. Acta, 43, p645, 2004.
M. Iza, M. Bousmina, R. Jerome - Rheol. Acta, 40, p10, 2001.
G. Schmidt, A. I. Nakatani, C. C. Han - Rheol. Acta, 41, p45, 2002.
S. E. Mall-Gleissle, W. Gleissle, G. H. McKinley, H. Buggisch - Rheol. Acta, 41, p61, 2002.
J. C. Majesté, C. Carrot, P. Stanescu - Rheol. Acta, 42, p437, 2003.
Yu. M. Samachenko, Z. R. Ul'berg, S. A. Komarskii, I. G. Kovzun, I. T. Protsenko - Colloid Journal, 65, p78, 2003.
T. V. Shevchenko, E. V. Ul'rikh, M. A. Yakovchenko, A. N. Pirogov, O. E. Smirnov - Colloid Journal, 66, p756, 2004.
Yu. M. Samachenko, Z. R. Ul'berg, S. A. Komarskii, I. G. Kovzun, I. T. Protsenko - Colloid Journal, 66, p150, 2004.
K. Kang, L. J. Lee, K. W. Koelling - Exp. In Fluids, 38, p222, 2005
|