LIPIDE
Lipidele reprezinta o clasa importanta de compusi naturali, larg raspandite in organismele vegetale si animale si de importanta majora pentru acestea. In general, se caracterizeaza prin solubilitate in solventi organici(eter etilic, acetona, benzen, cloroform, alcooli) si insolubilitate in apa.
In organisme lipidele indeplinesc rol plastic si energetic, participa la formarea membranelor biologice, la permeabilitatea celulara si la transportul diferitelor substa 646i85g nte liposolubile.
Exista numeroase clase de lipide care se deosebesc atat din punct de vedere al structurii moleculare, cat si prin gradul diferit de solubilitate in solventi organici, proprietate ce sta la baza extragerii si separarii acestora.
Din punct de vedere chimic, majoritatea sunt esteri naturali ai alcoolilor cu acizi grasi. Exista unele clase de lipide(sfingolipide), care desi contin in molecula aminoalcooli si acizi grasi, acestia nu se leaga intre ei prin legaturi esterice, ci peptidice, iar in cazul galactozilgliceridelor, legaturile sunt eterice.
In natura se gasesc atat in stare libera, predominant ca substante de rezerva in seminte, fructe, legume,tesutul adipos, in jurul organelor interne la animale, cat si asociate cu proteinele(lipoproteine) sau cu glucidele(glicolipide),care se gasesc in special in constituentii celulari cu activitate intensa.
Dupa compozitia chimica, lipidele se impart in lipide simple, formate din C,H si O,si lipide complexe, care contin in molecula si N,S sau P. Lipidele simple se impart la randul lor in mai multe clase: gliceride, ceride, steride, etolide, iar lipidele complexe cuprind urmatoarele doua clase mari:
-fosfatide(glicerofosfolipide,gliceroaminofosfolipide)
-sfingolipide(sfingofosfolipide,sfingoglicolipide, sfingoglicosulfolipide).
Cele mai importante produse alimentare bogate in lipide sunt: untul si margarina(80-85%), slanina(70%), untura(100%),uleiurile vegetale(98-100%),carnea grasa(15-30%),smantana(20%),branzeturile grase(20-30%),nucile si alunele(60-65%).
Reactiile de recunoastere ale diferitelor lipide sunt fie reactii caracteristice ale acizilor, fie ale alcoolilor sau ale unor componenti ce intra in componenta lor.
1. Reactii catalitice ale gliceridelor
1.1.Proba de acroleina, reactia de recunoastere a gliceridelor: Gliceridele sunt esteri ai glicerolului cu diferiti acizi grasi care se descompun la incalzire, punand in libertate - intre alti produsi de descompunere si glicerina. In prezenta substantelor deshidratante, ca de exemplu sulfatul acid de potasiu sau acidul boric, glicerolul se deshidrateaza la temperatura ridicata, transformandu-se in acroleina. Acroleina este o aldehida nesaturata care se poate recunoaste dupa mirosul ei caracteristic intepator si dupa reactia ce o da cu reactivul Tollens.
Formarea acroleinei are loc dupa urmatoarea reactie:

Glicerol Enol instabil Acroleina
1.2. Saponificarea gliceridelor si formarea sapunurilor
Gliceridele, principalele lipide simple, se desfac prin hidroliza in glicerol si acizi grasi. Daca hidroliza se realizeaza sub actiunea alcaliilor, se obtin sarurile acizilor grasi ,numite sapunuri.
Reactii chimice:

Glicerida Glicerol Sapun
1.3. Obtinerea acizilor grasi din sapunuri
Prin acidularea unei solutii de sapun sau de potasiu, se elibereaza acizii grasi conform regulii generale dupa care un acid este eliberat din sarurile sale prin tratarea cu un acid mai tare. Acizii grasi sunt insolubili in apa. In cazul palmitatului de sodiu se obtine acidul palmitic.
![]()
Palmitat de sodiu Acid palmitic
Proprietatile sapunurilor. Determinarea gradului de rancezire al unei grasimi
Sapunurile sunt saruri ale acizilor grasi(peste opt atomi de carbon) cu diferite metale, cel mai utilizat fiind cel de sodiu. Sapunurile au proprietati distincte de ale celorlalte saruri ale acizilor cu molecule mai mici. Astfel, solutiile diluate de sapun au o tensiune superficiala mult mai mica decat apa curata(25dyn/cm, fata de 72dyn/cm la apa). Aceasta comportare arata ca, in solutii foarte diluate, sapunurile sunt dizolvate sub forma de ioni individuali, RCOO- si Na+; cand concentratia depaseste un anumit nivel, anionii se unesc in numar mare, formand particule coloidale, de asociatie sau miceli.
Sapunurile se caracterizeaza prin aceea ca moleculele lor, de forma alungita, poseda la una din margini o grupa polara, hidrofila, in timp ce restul hidrocarbonat al moleculei este hidrofob. Datorita acestei structuri, moleculele de sapun, sau mai exact anionii lor, au tendinta de a se acumula la suprafata despartitoare a solutiei fata de mediu, orientandu-se cu grupa RCOO- inspre apa. Aceasta proprietate confera sapunurilor capacitatea de curatire.
Acumularea moleculelor de sapun pe interfata solutie-aer explica tensiunea superficiala mica a solutiilor de sapun si deci puterea mare de udare a acestor solutii.
Daca solutia de sapun vine in contact cu un lichid nemiscibil cu apa(grasime lichida, ulei mineral,etc.), moleculele de sapun se orienteaza perpendicular pe suprafata despartitoare, cu carboxilul spre apa si radicalul hidrocarbonat spre ulei. Prin aceasta se micsoreaza tensiunea superficiala a uleiului, care are tendinta acum de a-si mari suprafata; de aceea el se transforma(daca este agitat) in picaturi mici ce se imprastie in solutia de sapun; se formeaza o emulsie, sapunul jucand rol de emulgator.
Proprietatile sapunurilor
a)Solubilitatea: Sapunurile prezinta solubilitati diferite. Astfel, sapunurile de sodiu si potasiu se dizolva usor in apa calda si mai greu in apa rece. Solutiile obtinute au caracter coloidal, fapt ce se observa prin opalescenta solutiilor diluate si prin formarea de gel la racirea solutiilor mai concentrate.
b) Reactiile de substitutie
Sapunurile de calciu, magneziu si plumb se formeaza prin reactii de substitutie cu sapunurile solubile de sodiu, potasiu, litiu etc.
![]()
Sapun de sodiu Sapun de calciu
Aceste sapunuri sunt cu mult mai putin solubile in apa si se separa imediat sub forma de precipitat ,din care cauza apa dura nu formeaza spuma cu sapunul.
c) Proprietatile de emulsionare ale sapunurilor: Sapunul este o substanta cu insusiri capilare active deoarece moleculele de sapun au tendinta de a se aduna la suprafata despartitoare a solutiei fata de mediul inconjurator, intr-o anumita orientare.
Aceasta orientare se datoreaza prezentei in molecula a gruparii carboxilice hidrofile si a radicalului hidrocarburic hidrofob.
Datorita acumularii la suprafata despartitoare, se micsoreaza tensiunea superficiala a lichidului respectiv. Ca urmare a acestei proprietati, sapunurile se folosesc ca emulgatori.
Caracterul nesaturat al grasimilor
Datorita dublelor legaturi din moleculele acizilor grasi nesaturati, grasimile mai ales cele lichide au proprietati de aditie. Astfel, se pot aditiona hidrogen, oxigen ,halogeni, etc.
Caracterul nesaturat al grasimilor se poate pune in evidenta prin decolorarea solutiei de brom in cloroform.
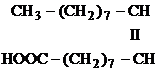 + Br2 ------>
+ Br2 ------> 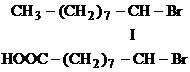
Acid oleic Acid dibromstearic
Determinarea gradului de rancezire a grasimii
Ca rezultat al aditiei oxigenului la dubla legatura a acizilor nesaturati ai gliceridelor se produce rancezirea, proces in care se formeaza peroxizi, aldehide si cetone. Gradul de rancezire, respectiv aparitia aldehidelor, se poate pune in evidenta prin diferite reactii de culoare.
Dupa gradul de rancezire apare o coloratie de la rosu la violet; cu cat grasimea este mai ranceda, culoarea va fi mai intensa.
Autooxidarea si Peroxidarea
Datorita unei configuratii electronice deosebite oxigenul molecular poseda o inertie chimica relativa, care poate fi invinsa in urma activarii in anumite conditii si producerii unor specii inalt reactive cum ar fi oxigen singlet, superoxid, hidroxil.
Autooxidarea in conceptia cea mai larga, de oxidare cu oxigenul atmosferic, cuprinde un domeniu foarte vast, din care peroxidarea constituie doar o parte. Pentru a preveni autooxidarea numeroaselor substante organice este necesara cunoasterea mecanismului acestui proces, mai ales in domeniul grasimilor , unde autooxidarea este foarte evidenta. Prima dovada a peroxidarii ca etapa initiala a autooxidarii a constituit-o izolarea unui hidroperoxid al ciclohexenei prin fotooxidare.
Peroxidarea constituie etapa initiala si principala a mecanismului de autooxidare care are loc sub actiunea oxigenului.
Datorita structurii electronice particulare, oxigenul are o comportare aparte, deoarece acceptarea unui electron va favoriza intrarea unui al doilea electron. In consecinta in peroxidare, oxigenul va fi un acceptor de electroni mai bun in stare activata decat in stare fundamentala si autooxidarile pot fi accelerate prin prezenta unor donori de electroni.
Studiul oxidarii grasimilor a furnizat substratul cel mai adecvat. Astfel s-a observat ca viteza de oxidare a sistemelor nesaturate cu punti metilen este mult mai mare decat in sistemele monoenice din cauza activarii unei grupe metilen intre doua duble legaturi adiacente. Aceasta activare mareste viteza de oxidare de 20-40 ori, demonstrand ca acizii polinesaturati sunt sursa principala a rancezirii oxidative a grasimilor.
Schema initierii peroxidarii

Procesul de autooxidare decurge dupa tipul reactiilor cu producere de radicali liberi. Reactia in lant poate fi initiata prin atacul oricarui radical liber asupra unui substrat favorabil, cei mai potriviti fiind radicalii formati prin descompunerea unui peroxid aflat in compozitia substratului ca impuritate. Astfel, cu cat decurge mai departe autooxidarea, aceasta isi genereaza propriul sau catalizator-peroxizii.
Natura autocatalitica a reactiei in lant poate fi oprita prin prezenta unor antioxidanti sau prin ciocnirea a doi radicali din care rezulta compusi inactivi.
|