PROTIDE
Protidele sunt cele mai importante substante naturale din organismele vii. Ele intra in alcatuirea protoplasmei si a nucleului celular si au rol structural si functional fundamental.
In organismele animale protidele reprezinta aproximativ 65-70% din materia uscata a acestora; in plante se gasesc intr-un procent mai mic, fiind cuprins intre 3-35%.
Sub aspectul compozitiei chimice,protidele sunt substante cuaternare, formate din cel putin patru elemente: C,H,O,N. Numeroase protide contin sulf, fosfor si unele metale(Fe,Cu,Mg,Mn).
Dupa reactia de hidroliza, protidele se impart in doua grupe mari:monoprotide si poliprotide. Monoprotidele se mai numesc si aminoacizi, sunt subst 747d33h ante simple, monomoleculare care nu hidrolizeaza.
Poliprotidele sunt substante formate din mai multe resturi de aminoacizi, unite prin intermediul legaturilor peptidice. Ele hidrolizeaza sub actiunea acizilor, bazelor sau enzimelor.
Din grupa poliprotidelor superioare fac parte proteinele si proteidele. Proteinele sunt formate numai din aminoacizi, iar proteidele contin in molecula lor si substante neproteice.
Proteinele se deosebesc de celelalte componente ale celulelor prin proprietati unice. Sunt proteine unele substante cu activitate biologica ale celulelor: enzimele, pigmentii respiratori, hormonii, anticorpii.
Se disting pe baza de solubilitate doua clase de proteine: insolubile(fibroase), care au functiunea de a conferi tesuturilor rezistenta mecanica si proteine solubile(globulare), care apar in celule in stare dizolvata sau sub forma de geluri hidratate, fiind solubile in apa sau solutii de electroliti.
Din prima clasa fac parte keratina, colagenul,miosina, fibroina. Acestea se dizolva numai in acizi sau baze concentrate, la cald, dar aceasta dizolvare este insotita de o degradare a macromoleculelor; din solutia obtinuta nu se mai regenereaza proteina initiala.
Din a doua clasa fac parte proteinele cu proprietati fiziologice specifice: proteinele din serul sanguin, enzimele, anticorpii, hormonii proteici si toxinele.
1. Reactii ale protidelor
1.1. Reactii de culoare: Reactiile de culoare pentru proteine se datoreaza fie intregii molecule proteice, fie anumitor aminoacizi componenti.
a). Reactii datorate intregii molecule proteice
 - Reactia ninhidrinei: Proteinele,
peptidele si aminoacizii incalziti in prezenta ninhidrinei dau
nastere la o coloratie albastra - violeta, care se
datoreaza gruparilor -NH2 libere. Reactia necesita deci
grupe -NH2 libere. Reactia poate servi si pentru developarea
cromatogramelor.
- Reactia ninhidrinei: Proteinele,
peptidele si aminoacizii incalziti in prezenta ninhidrinei dau
nastere la o coloratie albastra - violeta, care se
datoreaza gruparilor -NH2 libere. Reactia necesita deci
grupe -NH2 libere. Reactia poate servi si pentru developarea
cromatogramelor.
- Reactia biuretului
Aceasta reactie se bazeaza pe formarea unor chelati colorati intre substantele proteice si unele metale (Cu, Co, Ni). Numele reactiei provine de la biuret, substanta ce se formeaza din doua molecule de uree prin eliminare de NH3.
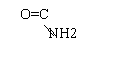
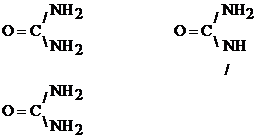
Reactia biuretului se datoreaza legaturii peptidice -CO-NH- si este pozitiva incepand cu tripeptidele. Peptidele dau o culoare rosie - violeta, proteinele o culoare violeta - albastra.
Sarurile de amoniu deranjeaza reactia, insa acest lucru se poate evita prin adaugarea unui exces de NaOH. Mecanismul acestei reactii consta in faptul ca legatura peptidica formeaza cu ionii Cu2+ complecsi solubili colorati.
Reactia este pozitiva si cu substantele care contin in molecula gruparea -CSNH2. Ionul de cupru poate fi inlocuit cu Ni sau Co. Reactia are sensibilitate de 1 : 10.000 si in conditii bine determinate, poate servi la dozarea colorimetrica a proteinelor.
b)Reactii de culoare datorate unor aminoacizi
Reactia xantoproteica: Proteinele care contin aminoacizi ciclici dau in prezenta acidului azotic si dupa o alcalinizare ulterioara, nitroderivati de culoare galben-portocalie.
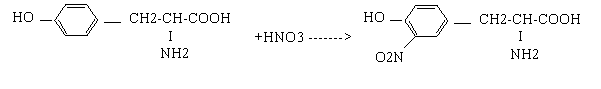
Tirozina Nitroderivat
O reactie similara se petrece cand cade pe piele o picatura de HNO3, se formeaza o pata galbena care nu se poate spala, deoarece sunt atacate chiar proteinele pieii.
Tirozina se coloreaza imediat, fenilalanina numai in prezenta acidului sulfuric concentrat, iar triptofanul da o culoare mai rosie. Majoritatea proteinelor contin in molecula lor aminoacizi ciclici si heterociclici, deci reactia este pozitiva la aproape toate proteinele.
- Reactia Millon (reactia tirozinei)
Reactia Milon are loc la tratarea solutiei unei proteine cu o solutie de azotat mercuric in acid azotic. Reactia se datoreaza prezentei aminoacizilor, ce contin o grupare fenolica (de exemplu tirozina) din molecula substantei proteice. Reactia nu este specifica intrucat este o reactie a fenolilor.
- Reactia triptofanului (reactia Adamkiewicz): Triptofanul reactioneaza in mediu acid cu diferite aldehide, dand compusi colorati. Gelatina si zeina fiind lipsite de triptofan, nu dau aceasta reactie.
Reactia argintinei (reactia Sakaguchi): Proteinele care contin in molecula lor un radical guanidinic dau in mediu alcalin in prezenta b-naftolului si a hipocloritului de sodiu complecsi colorati in rosu.
- Reactia datorata aminoacizilor cu sulf: Prin fierberea unei solutii proteice cu hidroxizi alcalini, sulful din aminoacizii cu sulf (cistina, cisteina, metionina), ce intra in componenta substantelor proteice, este pus in libertate sub forma de sulfura de sodiu. Anionul S2- poate fi pus in evidenta cu ajutorul sarurilor de plumb.
R - SH + 2NaOH = Na2S + R - OH + H2O
Na2S + Pb (CH3COO)2 = PbS + 2CH3-COONa
1.2. Reactii de precipitare a proteinelor
Reactiile de precipitare ale proteinelor servesc ca metoda de separare si de identificare a acestora. Cu toate ca sunt foarte variate ele se pot grupa astfel:
a) Reactii de precipitare reversibile, in care proteinele isi pastreaza structura moleculara nativa. Cu toate ca sunt foarte variate, ele se pot redizolva prin diferite metode.
Dintre precipitarile reversibile fac parte cele cu alcool diluat, acetona diluata, reactiile de salifiere si altele.
b) Reactii de precipitare ireversibile, in care are loc denaturarea proteinelor si alterarea structurii lor, asa incat nu mai pot reveni la structura initiala.
Dintre precipitarile ireversibile fac parte reactiile cu sarurile metalelor grele, cu reactivii alcaloizilor, coagularea prin fierbere si altele.
- Precipitarea cu alcool: Alcoolul si unii solventi organici fixeaza (extrag) apa care hidrateaza molecula proteinei; miceliile lipsite de apa flocuneaza.
Daca precipitatul obtinut este separat repede de alcool, proteina poate fi redizolvata in apa: precipitarea este deci reversibila. Denaturarea nu a avut timp sa se produca. Dupa un contact prelungit cu alcoolul, proteina se denatureaza si devine insolubila in apa. Variind concentratia alcoolului, pH-ul si temperatura de precipitare, diferitele proteine pot fi precipitate fractionat.
Salifierea proteinelor: sub influenta unor saruri de amoniu sau ale metalelor usoare are loc deshidratarea reversibila a miceliilor proteice. Prin diluarea cu apa a solutiilor, proteinele se solubilizeaza din nou. Metoda serveste pentru separarea fractionata a proteinelor.
- Precipitarea proteinelor cu acizi minerali: majoritatea acizilor minerali (sulfuric, clorhidric, metafosforic, azotic), precipita proteinele, iar acest precipitat se dizolva in exces de acid (exceptie face acidul azotic). Aceasta reactie ,utilizand acid azotic de diferite dilutii serveste la dozarea albuminelor din urina.
- Precipitarea proteinelor cu acizi organici: proteinele precipita cu acidul naftalinsulfonic, acidul tricloracetic si sulfosalicilic. Precipitarea cu acid tricloracetic se utilizeaza pentru indepartarea proteinelor din lichidele biologice, deoarece cu acest acid precipita numai proteinele.
Precipitarea proteinelor cu reactivul Esbach: acest reactiv este in mod curent folosit in clinica pentru depistarea si dozarea albuminelor din urina.
- Coagularea proteinelor: moleculele substantelor proteice au un caracter amfoter. In functie de concentratia ionilor de H+ din solutie, molecula se incarca cu sarcini pozitive sau negative. Concentratia ionilor de hidrogen la care molecula de proteina are un numar egal de sarcini pozitive si negative se numeste punct izoelectric. In majoritatea cazurilor constanta de disociere a proteinei ca acid, depaseste constanta de disociere a aceleiasi proteine ca baza. O particula pusa deci in solutie apoasa este incarcata de obicei negativ.
Prin acidularea treptata a unei astfel de solutii, gradul de disociere al proteinei ca baza se mareste (neutralizarea ionilor OH-). In acest mod se poate realiza o concentratie egala a ionilor pozitivi si negativi. La punctul izolelectric particulele coloidale devin electric neutre; solutia de proteina fiind putin stabila, precipita foarte usor.
Concentratia ionilor de hidrogen la care se realizeaza punctul izoelectric este o marime ce caracterizeaza proteina si care variaza intre limitele de pH 4,1 - 6,7.
|